题目内容
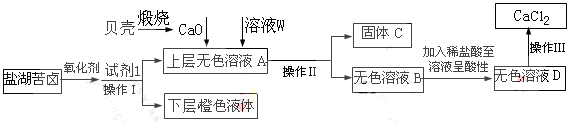
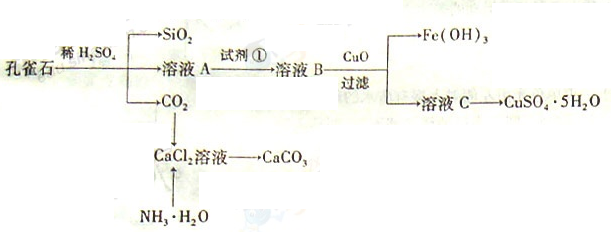
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下: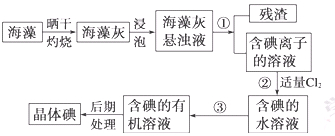
(1)指出操作③的名称: ;操作②中充入适量Cl2的目的是 。
(2)提取碘的过程中,可供选择的试剂是 ( )
| A.酒精 | B.四氯化碳 | C.汽油 | D.醋酸 |
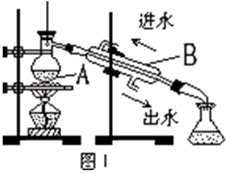
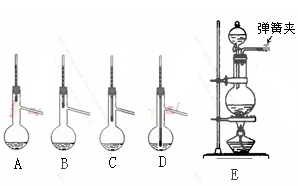
(3)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏。图I是某同学设计的蒸馏装置,图中明显的错误是 。
(4)有同学认为蒸馏时最好使用水浴加热,使用水浴的优点是: ;蒸馏结束,晶体碘聚集在 (填仪器名称)里。
(5) 实验③分离出来的废液中含有Cl–、SO42–,现只取一次试液,如何鉴别出Cl–、SO42–,依次加入试剂的为: 、 。
(6)某小组同学实验时需用到一定物质的量浓度的碘水溶液225mL,配制时需要的仪器除天平、玻璃棒、烧杯外,还需 、 。若摇匀时,发现液面低于刻度线,则配得溶液浓度(填偏大、偏小或无影响)。
(1)萃取(分液) 将I-充分氧化为I2,同时避免进一步氧化I2(2)BC
(3)冷凝管进出水的方向颠倒 未加碎瓷片(或沸石)
(4)均匀受热、便于控温,且加热温度不会过高 蒸馏烧瓶
(5)足量(硝酸酸化的)硝酸钡(没有足量不得分) 硝酸银溶液
(6)胶头滴管 250ml容量瓶 无影响
解析试题分析:(1)分离固体和液体用过滤,利用溶质在互不相溶的溶剂里溶解度不同,用一种溶剂把溶质从它跟另一种溶剂所组成的溶液里提取出来,这种方法叫做萃取,故③萃取;充入适量Cl2将I-充分氧化为I2,同时避免进一步氧化I2。
(2)萃取剂必须具备下列条件:碘在萃取剂中的溶解度大于在水中的溶解度,萃取剂和水不互溶,且萃取剂和碘不反应,四氯化碳和汽油符合条件;酒精和水能互溶,不能做萃取剂,故选BC;
(3)冷凝水应是下进上出,应加入适量碎瓷片防止暴沸。故答案为冷凝管进出水的方向颠倒、未加碎瓷片(或沸石)
(4)水浴加热的温度是使试管内或烧杯内试剂受热温度均匀,具有长时间加热温度保持恒定的特点,故答案为:均匀受热、便于控温,且加热温度不会过高;碘易升华,蒸馏结束,晶体碘聚集在蒸馏烧瓶。
(5)本题考查离子检验,Cl–用硝酸银溶液,SO42–用足量(硝酸酸化的)硝酸钡,但要注意顺序,先检验SO42–,再检验Cl–。故答案为足量(硝酸酸化的)硝酸钡、 硝酸银溶液。
(6)略。
考点:实验的基本操作,碘单质的提取

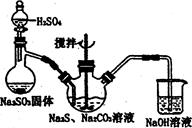
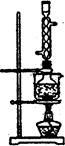
有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验。按右表所示的量和反应条件在三颈瓶中加入一定量P2O5,并注入95%的乙醇,并加热,观察现象。
| 实验 | P2O5 /g | 95%乙醇量/ mL | 加热方式 |
| 实验1 | 2 | 4 | 酒精灯 |
| 实验2 | 2 | 4 | 水浴70℃ |
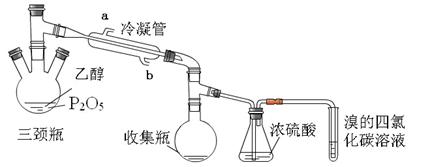
实验结果如下:
| 实验 | 实验现象 | ||
| 三颈瓶 | 收集瓶 | 试管 | |
| 实验1 | 酒精加入时,立刻放出大量的白雾,开始有气泡产生,当用酒精灯加热时,气泡加快生成并沸腾,生成粘稠状液体。 | 有无色液体 | 溶液褪色 |
| 实验2 | 酒精加入时,有少量白雾生成,当用水浴加热时,不产生气泡,反应一个小时,反应瓶内生成粘稠状液体 | 有无色液体 | 溶液不褪色 |
根据上述资料,完成下列填空。
(1)写出乙醇制乙烯的化学方程式 。
(2)上图装置中泠凝管的作用是___________,进水口为(填“a”或“b”)______,浓硫酸的作
用是 。
(3)实验1使溴的四氯化碳溶液褪色的物质是___________。
(4)实验2中,水浴加热所需仪器有 、 (加热、夹持仪器、石棉网除外)。
(5)三颈瓶、收集瓶中的液体经检验为磷酸三乙酯,写出三颈瓶中生成磷酸的化学方程式
_____________________,P2O5在实验1中的作用是______________________ 。
(6)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是____________
②P2O5与95%乙醇在加热条件下可以发生的有机反应的类型是________反应。
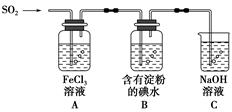




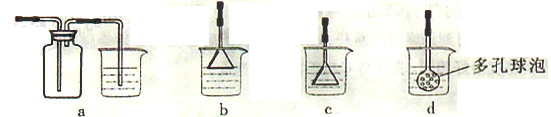
 CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):
CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):