题目内容
电化学在日常生活中用途广泛,图甲是镁—次氯酸钠燃料电池,电池总反应为Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含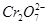 的工业废水的处理。下列说法正确的是
的工业废水的处理。下列说法正确的是
A.图乙中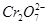 向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 向惰性电极移动,与该极近的OH-结合转化成Cr(OH)3除去 |
| B.图乙的电解池中,有0.084 g阳极材料参与反应,阴极会有336 mL的气体产生 |
| C.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓ |
| D.若图甲中3.6 g镁溶液产生的电量用以图乙废水处理,理论可产生10.7 g氢氧化铁沉淀 |
C
解析A项,在电解池中,阴离子应该移向阳极,根据装置乙可知,惰性电极做阴极;B项,未标明标准状况,故无法计算产生气体的体积;C项,根据装置甲可知,镁做负极,发生电极反应是Mg-2e-=Mg2+;D项,图甲中溶解3.6 g镁时,失去的电子是0.3 mol,在图乙中阳极反应是Fe-2e-=Fe2+,根据电子守恒可得此时生成的Fe2+是0.15 mol,所以最后生成的氢氧化铁也是0.15 mol即16.05 g。

 步步高达标卷系列答案
步步高达标卷系列答案已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用右图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL。下列说法正确的是( )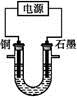
| A.铜电极连接电源正极 |
| B.黑色粉末X是铁粉 |
C.铜的相对原子质量的计算式是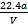 |
D.石墨电极上发生的反应是4OH--4e- O2↑+2H2O O2↑+2H2O |
关于如图所示各装置的叙述中,正确的是
| A.装置①是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
| B.装置①中,铁作负极,电极反应式为:Fe3++e-=Fe2+ |
| C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深 |
| D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是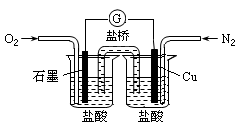
| A.此装置能将化学能转变为电能 |
| B.石墨电极的反应式:O2+2H2O+4e—=4OH— |
| C.电子由Cu电极经导线流向石墨电极 |
| D.电池总的反应是:2Cu+O2+4HCl=2CuCl2+2H2O |
下列有关电池的说法不正确的是
| A.手机上用的锂离子电池属于二次电池 |
| B.铜锌原电池工作时,电子沿外电路从铜电极流向锌电极 |
| C.甲醇燃料电池可把化学能转化为电能 |
| D.锌锰干电池中,锌电极是负极 |
为防止钢铁锈蚀,下列防护方法中正确的是( )
| A.在精密机床的铁床上安装铜螺钉 |
| B.在排放海水的钢铁阀门上用导线连接一块石墨,一同浸入海水中 |
| C.在海轮舷上用铁丝系住锌板浸在海水里 |
| D.在电动输油管的铸铁管上接直流电源的正极 |
固体电解质是具有与强电解质水溶液的导电性相当的一类无机固体。这类固体通过其中的离子迁移进行电荷传递,因此又称为固体离子导体。目前固体电解质在制造全固态电池及其他传感器、探测器等方面的应用日益广泛。如RbAg4I5晶体,其中迁移的物种全是Ag+,室温导电率达0.27 Ω-1·cm-1。利用RbAg4I5晶体,可以制成电化学气敏传感器。下图是一种测定O2含量的气体传感器示意图,被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是 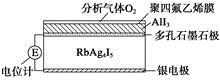
| A.I2+2Rb++2e-=2RbI | B.I2+2Ag++2e-=2AgI |
| C.Ag-e-=Ag+ | D.4AlI3+3O2=2Al2O3+6I2 |
将KCl和CuSO4两种溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如图所示,则下列说法正确的是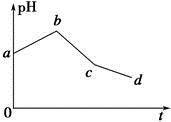
| A.整个过程中两电极反应2Cl--2e-=Cl2↑、2H++2e-=H2↑不可能同时发生 |
| B.电解至c点时,往电解液中加入适量CuCl2固体,即可使电解液恢复至原来的浓度 |
| C.ab段表示电解过程中H+被还原,pH上升 |
| D.原混合溶液中KCl和CuSO4的浓度之比恰好为2∶1 |
如图所示,X为单质硅,Y为金属铁,a为NaOH溶液,组装成一个原电池,下列说法中正确的是( )
A.X为负极,电极反应为:Si-4e- Si4+ Si4+ |
B.X为正极,电极反应为:4H2O+4e- 4OH-+2H2↑ 4OH-+2H2↑ |
C.X为负极,电极反应为:Si+6OH--4e- Si+3H2O Si+3H2O |
D.Y为负极,电极反应为:Fe-2e- Fe2+ Fe2+ |