题目内容
4.下列有关化学用语表示正确的是( )| A. | 二氧化硅的分子式:SiO2 | |
| B. | 熔融状态下硫酸氢钾的电离方程式:KHSO4$\frac{\underline{\;熔融\;}}{\;}$K++HSO4- | |
| C. | 甲基的电子式: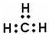 | |
| D. | HClO的结构式:H-Cl-O |
分析 A.二氧化碳晶体为原子晶体,不存在分子式;
B.融融硫酸氢钾电离出钾离子和硫酸氢离子;
C.甲基为中性原子团,碳原子最外层为7个电子;
D.次氯酸中不存在H-Cl键,中心原子为O原子.
解答 解:A.SiO2为而二氧化硅的化学式,二氧化硅为原子晶体,不存在分子式,故A错误;
B.熔融状态下硫酸氢钾电离出钾离子和硫酸氢根离子,其电离方程式为:KHSO4$\frac{\underline{\;熔融\;}}{\;}$K++HSO4-,故B正确;
C.甲烷去掉1个H原子剩余部分为甲基,甲基为电中性基团,碳原子有1个单电子,电子式为 ,故C错误;
,故C错误;
D.HClO的中心原子为O,分子中存在1个氧氢键和1个O-Cl键,其正确的结构式为:H-O-Cl,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、分子式与化学式、结构式等知识,明确常见化学用语的表示方法为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
15.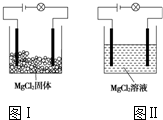 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
 某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )| A. | MgCl2是非电解 | |
| B. | MgCl2溶液是电解质 | |
| C. | MgCl2在水溶液中电离出了可以自由移动的离子 | |
| D. | MgCl2只有在溶液中才能导电 |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 48克O2和O3的混合物含有氧原子数3NA | |
| B. | 22.4L甲烷(CH4)所含的原子数为5NA | |
| C. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA | |
| D. | 在20℃,1.01×105Pa(即在标准状况)时,11.2L氧气所含的原子数为NA |
9.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、SO32- | |
| B. | 饱和氯水中:Cl-、NO3-、Na+、SO32- | |
| C. | c(H+)=1×10-1 mol•L-1的溶液中:Cu2+、Al3+、SO42-、NO3- | |
| D. | 0.1mol•L-1CH3COONa溶液:H+、Al3+、Cl-、NO3- |
16.化学与环境密切相关,下列有关说法正确的是( )
| A. | CO2属于大气污染物 | |
| B. | 酸雨是pH小于7的雨水 | |
| C. | 大气中CO2含量的增加会导致温室效应加剧 | |
| D. | CO2、NO2或SO2都会导致酸雨的形成 |
13.HA为酸性略强于醋酸的一元弱酸,则下列叙述正确的是( )
| A. | 0.1 mol•L-1 HA溶液与0.1 mol•L-1 NaOH溶液混合至溶液呈中性:c(Na+)>c(A-) | |
| B. | 0.1 mol•L-1 HA溶液中:c(H+)=c(OH-)+c(A-) | |
| C. | 0.1 mol•L-1 NaA溶液中:c(Na+)>c(OH-)>c(A-)>c(H+) | |
| D. | 0.1 mol•L-1 HA溶液中加入少量NaA固体,HA的电离常数减小 |
14.化学实验有助于理解化学知识,形成化学观念.下列实验操作正确的是( )
| A. |  称量药品 | B. | 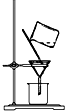 过滤 | C. | 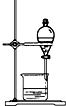 分离乙醇和水 | D. | 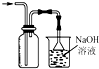 收集氯气 |