题目内容
15.(1)完成下列物质的电子式A.Na+Na+,B.Cl-
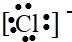 ,C.H2O
,C.H2O ,D.Na2O2
,D.Na2O2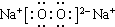 ,
,(2)用电子式表示下列化合物的形成过程
H2O
 ;MgCl2
;MgCl2 .
.
分析 (1)A、钠离子为简单阳离子;
B、氯离子为阳离子,最外层为8电子稳定结构;
C、水分子中氧原子与2个氢原子共用2对电子对;
D、Na2O2是离子化合物;
(2)根据各种物质的类别判电子式的不同,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构.
解答 解:(1)A、钠离子为简单阳离子,离子符号即为电子式,故答案为:Na+;
B、氯离子为阳离子,最外层为8电子稳定结构,电子式为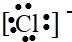 ,故答案为:
,故答案为: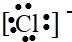 ;
;
C、水分子中氧原子与2个氢原子共用2对电子对,电子式为 ,故答案为:
,故答案为: ;
;
D、过氧化钠是离子化合物,电子式为: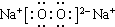 ,故答案为:
,故答案为: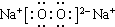 ;
;
(2)H2O为共价化合物,各原子达到稳定结构,用电子式表示形成过程为 ;
;
MgCl2为离子化合物,用电子式表示的形成过程为 ,
,
故答案为: ;
; .
.
点评 本题考查用电子式的形成过程,题目难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
5.实验室制取氯气应该选用哪一套装置( )
| A. |  | B. |  | C. |  |
20.下列关于接触法制硫酸的叙述中,正确的是( )
| A. | 用硫代替硫铁矿可以避免对环境的污染 | |
| B. | 接触室中的热交换器是为预热反应物和冷却生成物、节约能量而设计的 | |
| C. | 吸收塔中气体和浓H2SO4一起从塔顶端进入生成成品酸 | |
| D. | 用水吸收SO3使之成为硫酸 |
7.下列关于丙烯(CH3-CH═CH2)的说法正确的( )
| A. | 丙烯分子有8个σ键,1个π键 | |
| B. | 丙烯分子中3个碳原子都是sp3杂化 | |
| C. | 丙烯分子中只存在极性键 | |
| D. | 丙烯分子中3个碳原子在同一直线上 |
4.某化学反应过程中的能量变化关系如图所示,下列结论正确的是( )
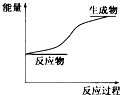

| A. | 生成物的总能量小于反应物的总能量 | |
| B. | 断开化学键所吸收的能量小于形成化学键所放出的能量 | |
| C. | 该反应可能是酸和碱的中和反应 | |
| D. | 该反应中其他形式的能量转化成了化学能 |
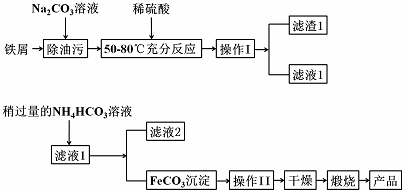
5.如图是实验室常见的气体制取、干燥和收集装置.若用过氧化氢和二氧化锰来制取干燥的氧气,则合理的装置组合为( )


| A. | ①⑤⑥ | B. | ②④⑥ | C. | ②⑤⑦ | D. | ③④⑦ |
 ;
;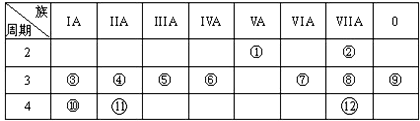
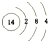 ,写出①的气态氢化物分子的电子式
,写出①的气态氢化物分子的电子式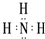 .
.