题目内容
1.常温下,四个容积为20L的容积中分别装有质量相同的下列气体,产生的压强最大的是( )| A. | Cl2 | B. | HCl | C. | SO2 | D. | CO2 |
分析 相同温度下,质量、体积相同的不同气体,其压强与物质的量成正比,如果产生的压强最大,则气体的物质的量最大即可,根据n=$\frac{m}{M}$计算.
解答 解:相同温度下,质量、体积相同的不同气体,其压强与物质的量成正比,如果产生的压强最大,则气体的物质的量最大即可,根据n=$\frac{m}{M}$知,相同质量时n、M成正比,n最大时M最小,Cl2、HCl、SO2、CO2的摩尔质量分别是71g/mol、36.5g/mol、64g/mol、44g/mol,摩尔质量最小的是氯化氢气体,所以压强最大的是氯化氢,
故选B.
点评 本题考查阿伏伽德罗定律及其推论,侧重考查分析能力,明确物质的量公式中各个物理量之间的关系式是解本题关键,题目难度中等.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
11.下列物质中,其水溶液能导电,但属于非电解质的是( )
| A. | 硫酸 | B. | Cl2 | C. | NH4NO3 | D. | NH3 |
12.质量相等的SO2和SO3,所含氧原子数之比为( )
| A. | 1:1 | B. | 2:3 | C. | 6:5 | D. | 5:6 |
9.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 7.8 g Na2O2中含有的阴离子数为0.2NA | |
| B. | 由NO2、O2组成的混合物中共有NA个分子,则其中的氧原子数目为2NA | |
| C. | 1 mol•L-1的NH4Cl溶液中的NH${\;}_{4}^{+}$的数目小于NA | |
| D. | 铜与浓硫酸反应中,当转移的电子数为0.2NA时,生成的SO2为2.24 L |
13.下列说法不正确的是( )
①凡是易溶于水的化合物都可以写成离子形式
②凡是强电解质,在离子方程式中都要以离子形式表示
③复分解反应中,离子反应总是向着溶液中反应物离子浓度减少的方向进行,任何一种离子的浓度在离子反应中一定变小
④单质和氧化物在离子方程式中不能用离子符号表示
⑤凡是酸都可以在离子方程式中用H+表示
⑥参加离子反应的物质一定都是电解质.
①凡是易溶于水的化合物都可以写成离子形式
②凡是强电解质,在离子方程式中都要以离子形式表示
③复分解反应中,离子反应总是向着溶液中反应物离子浓度减少的方向进行,任何一种离子的浓度在离子反应中一定变小
④单质和氧化物在离子方程式中不能用离子符号表示
⑤凡是酸都可以在离子方程式中用H+表示
⑥参加离子反应的物质一定都是电解质.
| A. | ①②③ | B. | ③④⑤ | C. | ②③⑤⑥ | D. | ①②③⑤⑥ |
9.下列实验方法或操作不正确的是( )
| A. | 蒸馏实验中,为了防止暴沸,要在蒸馏烧瓶中加入沸石 | |
| B. | 可用丁达尔效应区别溶液和胶体 | |
| C. | 用CCl4萃取碘水后分液时,先打开分液漏斗活塞,放出下层液体,再关闭活塞,从漏斗上口倒出上层液体 | |
| D. | 检验某溶液中是否含有Fe2+时,可先加入适量的氯水,再滴加硫氰化钾溶液,若溶液变为红色,则说明溶液中一定含有Fe2+ |
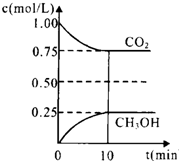 二氧化碳是引起“温室效应”的主要物质,节能减排、高效利用能源,能够减少二氧化碳的排放.在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
二氧化碳是引起“温室效应”的主要物质,节能减排、高效利用能源,能够减少二氧化碳的排放.在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-a kJ•mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
 .
.