��Ŀ����
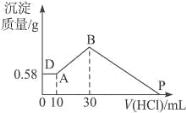
����Ŀ����1����Mg��Al��Ϸ�ĩ10.2 g����50 mL 4 mo1��L��1�����ᣬ������2mo1��L��1������������Һ��ʹ�ó����ﵽ���������������������Ƶ����Ϊ_____mL��
��2����״���£���������ZnͶ�뵽һ������Ũ�����У���ȫ��Ӧ���ռ���336 mL���壬��������ͨ��������ˮ�У�Ȼ���������BaCl2��Һ�����ʵ�������ø������2.33 g���ɴ���֪��������SO2���������Ϊ________��
��3��ij��ѧѧϰС���ڽ���֪ʶ����ʱ�������¹��ɣ���Щ��Ӧ������Һ��Ũ��ϡ�����ܵ��������������ʱ��������ݴ��ⶨ�����¼��������Ŀ�����������Ӧ�𰸡�
I��ʵ������ȡ�����Ļ�ѧ����ʽΪMnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2����MnO2��������ϡ���ᣩ�����������ַ�����ȡ���������ú�HCl 146 g��Ũ������������MnO2��Ӧ������87 g MnO2��������Ũ���ᷴӦ��������HCl�Ļӷ��������ַ������ɵ����������Ƿ�����____���������������������������������ڡ�
MnCl2��2H2O��Cl2����MnO2��������ϡ���ᣩ�����������ַ�����ȡ���������ú�HCl 146 g��Ũ������������MnO2��Ӧ������87 g MnO2��������Ũ���ᷴӦ��������HCl�Ļӷ��������ַ������ɵ����������Ƿ�����____���������������������������������ڡ�
II����100 mL��18 mo1��L��1��Ũ������������ͭ��ַ�Ӧ����Һ����������ӵ����ʵ���____����������������������������0.9 mol��
���𰸡�100 66.7% �� ��
��������
(1)����2mol/L������������Һ��Ҫʹ�����ij�����������������Ϊ������þ��������������ʱ��ҺΪ�Ȼ�����Һ���������������������غ�����������Ƶ����ʵ����������������������
(2)����BaSO4���������������ʵ������ٽ��ԭ���غ��SO2��������ʵ�������������������SO2�����������
(3)I������MnO2��ŨHCl��Ӧ�����ŷ�Ӧ�Ľ��У�ŨHCl��ϡ��ϡ�������MnO2��Ӧ��MnO2����ʱ������ȷ���������������Ũ��������ʱ���ܸ���MnO2���������������������
II��ͭ��Ũ���ᷴӦ���ŷ�Ӧ�Ľ��У�Ũ�����ϡ��ͭ��ϡ�����Ӧ��
(1)Ҫʹ�����ij�����������������Ϊ������þ��������������ʱ��ҺΪ�Ȼ�����Һ���������������������غ��֪��n(NaOH)=n(NaCl)=n(HCl)=0.05L��4mol/L=0.2mol������������������Һ�����Ϊ![]() =0.1L=100mL��
=0.1L=100mL��
(2)2.33 gBaSO4�����ʵ���Ϊ![]() =0.01mol����ԭ���غ�֪���������SO2�����ʵ���Ϊ0.01mol����״���µ����Ϊ0.01mol��22.4L/mol=0.224L=224mL�����������SO2���������Ϊ
=0.01mol����ԭ���غ�֪���������SO2�����ʵ���Ϊ0.01mol����״���µ����Ϊ0.01mol��22.4L/mol=0.224L=224mL�����������SO2���������Ϊ![]() =66.7%��
=66.7%��
(3)I��146 g HCl�����ʵ���Ϊ![]() =4mol��87 g MnO2�����ʵ���Ϊ
=4mol��87 g MnO2�����ʵ���Ϊ![]() =1mol������MnO2��ŨHCl��Ӧ�����ŷ�Ӧ�Ľ��У�ŨHCl��ϡ��ϡ�������MnO2��Ӧ��MnO2����ʱ������ȷ������������������MnO2��4HCl(Ũ)
=1mol������MnO2��ŨHCl��Ӧ�����ŷ�Ӧ�Ľ��У�ŨHCl��ϡ��ϡ�������MnO2��Ӧ��MnO2����ʱ������ȷ������������������MnO2��4HCl(Ũ)![]() MnCl2��2H2O��Cl2����֪��Ӧ���в���������С��1mol����Ũ��������ʱ����Ӧ�ڸ���MnO2�������������������Ϊ1mol�������ַ������ɵ����������Ƿ����٣��ڣ�
MnCl2��2H2O��Cl2����֪��Ӧ���в���������С��1mol����Ũ��������ʱ����Ӧ�ڸ���MnO2�������������������Ϊ1mol�������ַ������ɵ����������Ƿ����٣��ڣ�
II��100 mL��18 mo1��L��1��Ũ������������H2SO4�����ʵ���Ϊ18mol/L��0.1L=1.8mol��ͭ��Ũ���ᷴӦ��Cu+2H2SO4(Ũ)![]() CuSO4+SO2��+2H2O������ԭ��Ũ����Ϊ�μӷ�Ӧ��Ũ�����һ�룬���ŷ�Ӧ�Ľ��У�Ũ�����ϡ��ͭ��ϡ�����Ӧ���ʲμӷ�Ӧ������С��1.80mol����ԭ����������ʵ���С��0.900mol����ԭ���غ��֪��ַ�Ӧ����Һ����������ӵ����ʵ�����1.8mol-0.9mol=0.9 mol��
CuSO4+SO2��+2H2O������ԭ��Ũ����Ϊ�μӷ�Ӧ��Ũ�����һ�룬���ŷ�Ӧ�Ľ��У�Ũ�����ϡ��ͭ��ϡ�����Ӧ���ʲμӷ�Ӧ������С��1.80mol����ԭ����������ʵ���С��0.900mol����ԭ���غ��֪��ַ�Ӧ����Һ����������ӵ����ʵ�����1.8mol-0.9mol=0.9 mol��