题目内容
【题目】氢能被视为最具发展潜力的清洁能源,开发新型储氢材料是氢能利用的重要研究方向。请回答下列问题:
Ⅰ.化合物A(H3BNH3)是一种潜在的储氢材料,可由六元环状物质(HB=NH)3通过如下反应制得:3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3。
(1)基态B原子的价电子排布式为_____,B、C、N、O第一电离能由大到小的顺序为_____,CH4、NH3、CO2的键角按照由大到小的顺序排列为_____。
Ⅱ.氢气的安全贮存和运输是氢能应用的关键。
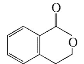
(1)印度尼赫鲁先进科学研究中心的Datta和Pati等人借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种材料的分子呈平面结构(如图),每个杂环平面上下两侧最多可吸附10个H2分子。
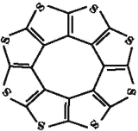
①S的基态原子中能量最高的电子,其原子轨道呈_____形。
②C16S8与H2微粒间的作用力是_____。
③C16S8分子中C原子和S原子的杂化轨道类型分别为_____。
【答案】2s22p1 N>O>C>B CO2>CH4>NH3 哑铃形(纺锤形) 范德华力(分子间作用力) sp2、sp3
【解析】
Ⅰ.(1)B是5号元素,核外有5个电子,根据构造原理书写该原子的价电子排布式为2s22p1。同一周期电离能随着原子序数增大而呈增大趋势,但是第ⅡA族、第ⅤA族的第一电离能大于其相邻元素,所以B、C、N、O第一电离能由大到小的顺序为N>O>C>B。CH4、NH3、CO2的空间构型分别为正四面体、三角锥形、直线形,孤电子对之间的排斥力>孤电子对和成键电子对之间的排斥力>成键电子对之间的排斥力,这三种分子孤电子对个数分别是0、1、0,结合其空间构型判断键角由大到小的顺序排列为CO2>CH4>NH3。故本题答案为:2s22p1;N>O>C>B;CO2>CH4>NH3;
Ⅱ.(1)①S元素位于第三周期,第ⅥA族,价电子排布式为3s23p4,能量最高的能级是3p,其原子轨道呈哑铃形(纺锤形),故本题答案为:哑铃形(纺锤形);
②C16S8与H2都是分子晶体,微粒间的作用力是范德华力(分子间作用力),故本题答案为:范德华力(分子间作用力);
③根据上图可知,C原子采取sp2杂化,S原子采取sp3杂化,故本题答案为:sp2、sp3。

 阅读快车系列答案
阅读快车系列答案【题目】硫化氢(H2S)是一种无色具有臭鸡蛋气味、能溶于水的高毒性的化合物,其广泛存在化石燃料加工的尾气中。为避免污染环境,可用活性炭材料进行脱硫,脱硫的方法有物理吸附法、化学吸附法和氧化法。
(1)物理吸附法:
物理吸附法是先将尾气缓缓通过活性炭,将H2S从尾气中转移到活性炭的微孔或表面,这是利用活性炭的___性。
(2)氧化法:
利用吸附在活性炭表面上的活性氧(O),将H2S氧化成S而除去,该反应的化学方程式是___。
(3)化学吸附法:
①利用H2S能溶于水,形成硫化氢溶液,更易被活性炭吸附。若0.1molL-1H2S的pH约为4,则H2S在水溶液中的电离方程式是___,被吸附的离子主要有___。
②工业生产中用CuCl2溶液处理活性炭的工艺称为活性炭的改性,改性后的活性炭能提高化学吸附法中H2S的吸收量。
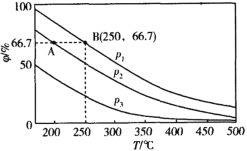
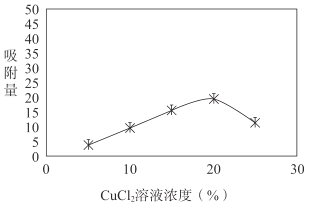
i.用不同浓度的CuCl2溶液改性后的活性炭对H2S吸附量的影响如图所示。随着CuCl2溶液浓度的升高,活性炭对硫化氢吸附量不再增加,原因是过多金属离子阻塞活性炭内部的微孔结构,导致活性炭的吸附能力下降。改性后的活性炭,能提高H2S吸附量的原因是___(用离子方程式表示)。
ii.水膜处理对活性炭吸附H2S量也有影响。测定含水量不同时,活性炭对硫化氢吸附量的影响,实验结果如下表。
载水率(%) | 0 | 5.32 | 10.23 | 15.33 | 20.19 |
吸附量(mg/g—活性炭) | 19.62 | 21.52 | 32.42 | 31.28 | 30.78 |
注:载水率即单位质量的活性炭吸附水的质量。
活性炭载水率为10%以上时,吸附量降低,其可能的原因是___。
(4)下列关于活性炭处理H2S尾气的说法正确的是___(选填字母序号)。
a.化学吸附过程中存在着电离平衡的移动
b.活性炭改性时,CuCl2溶液的浓度越大,H2S的吸附量越大
c.其他条件相同时,低温、缓慢通入尾气更有利于H2S的物理吸附
d.适当提高活性炭的载水率,可提高H2S吸附量的原因是活性炭吸附离子比吸附分子能力更强
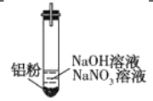
【题目】某无色溶液中可能含有H+、OH-、Na+、K+、NO![]() ,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。
,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。
(1)甲同学分析“若H+大量存在,则NO![]() 就不能大量存在”,设计实验证实如下:
就不能大量存在”,设计实验证实如下:
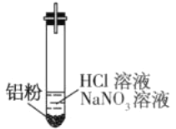
装置 | 现象 |
| Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,液面上方出现浅棕色气体 Ⅲ.试管变热,溶液沸腾 |
①现象Ⅲ产生的原因___。
②根据现象Ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
实验 | 内容 | 现象 |
实验1 | 将湿润KI—淀粉试纸置于空气中 | 试纸未变蓝 |
实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
实验1、2说明反应生成了NO。
请用化学方程式解释气体变为浅棕色的原因___。
(2)乙同学分析“若OH-大量存在,NO![]() 也可能不大量存在”,重新设计实验证实如下:
也可能不大量存在”,重新设计实验证实如下:
装置 | 现象 |
| Ⅰ.实验初始,未见明显现象 Ⅱ.过一会儿,出现气泡,有刺激性气味 |
为确认:"刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
产生该刺激性气味气体的离子方程式是___。
(3)甲、乙两位同学设计的实验初始时均未见明显现象的原因是___。
(4)根据以上实验分析,该溶液中一定大量存在的离子是___。