题目内容
7.下列离子方程式中正确的是( )| A. | 向NaHSO4溶液中滴加Ba(OH)2至SO42-沉淀完全:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O | |
| B. | 碳酸钠溶液与醋酸反应:CO32-+2H+=CO2↑+H2O | |
| C. | 氢氧化亚铁与硝酸混合:Fe(OH)2+2H+=Fe2++2H2O | |
| D. | 将1~2mL氯化铁饱和溶液加到20mL沸水中:Fe3++3H2O?Fe(OH)3(胶体)+3H+ |
分析 A.参加反应的n(H+):n(SO42-)=1:1;
B.醋酸为弱酸,应写成化学式;
C.硝酸具有强氧化性,可氧化亚铁离子;
D.氯化铁在加热条件下可水解生成氢氧化铁胶体.
解答 解:A.参加反应的n(H+):n(SO42-)=1:1,离子方程式为H++SO42-+Ba2++OH-=BaSO4↓+H2O,故A错误;
B.醋酸为弱酸,应写成化学式,离子方程式为CO32-+2HAc=CO2↑+2Ac-+H2O,故B错误;
C.硝酸具有强氧化性,可氧化亚铁离子,离子方程式为3Fe(OH)2+NO3-+10H+=3Fe3++8H2O+NO↑,故C错误;
D.氯化铁在加热条件下可水解生成氢氧化铁胶体,离子方程式为Fe3++3H2O?Fe(OH)3(胶体)+3H+,故D正确.
故选D.
点评 本题考查了离子方程式的正误判断,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,注意把握离子的性质以及反应的物质的量的关系.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
18.已知以下化学键的键能:H-H 436kJ/mol,Cl-Cl 243kJ/mol,H-Cl 431kJ/mol.下列叙述正确的是( )
| A. | Cl-Cl键比H-H键的键能小,是因为Cl原子比H原子的非金属性强 | |
| B. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=183 kJ/mol | |
| C. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=-183 kJ/mol | |
| D. | H2(g)与Cl2(g)反应生成1 molHCl(g),反应的△H=-183 kJ/mol |
15.背景材料:(1)重庆工商及警方查获灌注重晶石粉的活鸡近千只.(2)台湾查获饮料食品违法添加有毒塑化剂一邻苯二甲酸酯(DEHP).(3)铅中毒被视为当今儿童智能发育的“第一杀手”.(4)日本福岛第一核电站造成含131I的放射性物质泄漏.下列有关说法正确是( )
| A. | 重晶石的主要成分是硫酸钡,可溶于胃酸 | |
| B. | 塑化剂和塑料都是高分子化合物 | |
| C. | 82Pb位于周期表第六周期IVA族 | |
| D. | 碘元素的相对原子质量是131 |
2.有两种气态不饱和烃的混合物共20mL,完全燃烧可生成H2O蒸气72mL和CO276mL(气体体积均在同温同压下测定),则这两种烃的分子式为( )
| A. | C2H4、C4H8 | B. | C2H2、C3H8 | C. | C3H4、C4H8 | D. | C3H4、C3H8 |
12.下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
| A. | 液氟的气化和液溴的气化 | B. | 干冰和氯化铵分别受热变为气体 | ||
| C. | 二氧化硅和铁分别受热熔化 | D. | 食盐和葡萄糖分别溶解在水中 |
19.某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、CO32-、HCO3-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入少量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是( )
| A. | 若向该溶液中加入过量的稀硫酸,溶液中阴离子种类仍不变 | |
| B. | 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 该溶液中一定不含Al3+、Ba2+、Cl- |
16.下列各组离子在溶液中按括号内的物质的量之比混合,得到无色、碱性、澄清溶液的是( )
| A. | Na+、Al3+、Cl-、OH-(5:2:7:4) | B. | NH4+、Ba2+、OH-、Cl-(1:1:1:2) | ||
| C. | Fe3+、Na+、Cl-、S2-(1:2:3:1) | D. | K+、H+、I-、HCO3-(1:1:1:1) |
9.如图所示是一个有机物的核磁共振氢谱图,请你观察图谱,分析其可能是下列物质中的( )
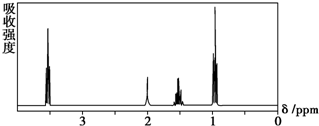

| A. | CH3CH2CH2CH3 | B. | (CH3)2CHCH3 | C. | CH3CH2CH2OH | D. | CH3CH2COOH |