题目内容
T ℃时,有甲、乙两个密闭容器,甲容器的体积为1 L,乙容器的体积为2 L,向甲、乙两容器中都加入5 mol A和3 mol B,发生如下反应:3A(g)+ bB(g)试回答下列问题:?
(1)在这2 min内,甲容器中B的化学反应速率为___________,化学方程式中化学计量数b=________。
(2)T ℃时,在另一个体积与乙相同的丙容器中,起始时加入3 mol C和1 mol D,为使达到平衡时B的浓度仍然为0.6 mol·L -1,则还需加入___________mol A和____________mol B。
(3)若要使甲、乙容器中B的平衡浓度相等,可以采取的措施是____________(填序号)。
A.保持温度不变,增大甲容器的体积至2 L?
B.保持容器体积不变,使甲容器升高温度?
C.保持容器体积和温度都不变,向甲容器中加入一定量的A气体?
D.保持容器体积和温度都不变,向甲容器中加入一定量的B气体
(1)1 mol·(L·min) -1? 2?
(2)2 1?
(3)AC?
解析:(1)B的反应速率应为 =1 mol·L -1·min -1,
=1 mol·L -1·min -1,
v(A)= =1.5 mol·L -1·min -1.
=1.5 mol·L -1·min -1.
(2)乙为等容变化,根据等效平衡原理加入物质与原来相当,即5 mol A和3 mol B,而现加入3 mol C和1 mol D,相当于3 mol A和2 mol B,故还应加A 2 mol、B 1 mol。?
(3)由于甲比乙体积小,故甲达平衡时与乙相比平衡左移B的浓度为乙中B浓度的1~2倍,因而必须再使平衡向右移动,可加入A或增大容积为原来的2倍。

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
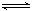 3C(g)+2D(g),
3C(g)+2D(g),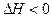 ;4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:
;4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题: 3C(g)+2D(g),
3C(g)+2D(g),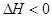 ;4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:
;4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题: