题目内容
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol甲基(-CH3)中含有电子的数目为10NA |
| B、1mol乙醇在O2中完全燃烧,电子转移数目为12NA |
| C、1mol苯乙烯中含有的C=C数为4NA |
| D、标准状况下,11.2L的己烷所含的分子数为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据甲基是中性取代基,结合结构计算所含电子数;
B、依据乙醇燃烧生成二氧化碳和水的反应定量关系计算电子转移;
C、苯分子中无碳碳双键;
D、标准状况己烷不是气体.
B、依据乙醇燃烧生成二氧化碳和水的反应定量关系计算电子转移;
C、苯分子中无碳碳双键;
D、标准状况己烷不是气体.
解答:
A、依据甲基是中性取代基,结合结构计算1mol甲基(-CH3)中含有电子的数目为9NA,故A错误;
B、依据乙醇燃烧生成二氧化碳和水的反应定量关系计算电子转移,1mol乙醇在O2中完全燃烧,C2H6O+3O2→2CO2+3H2O,电子转移数目为12NA,故B正确;
C、苯分子中无碳碳双键,故C错误;
D、标准状况己烷不是气体,11.2L的己烷物质的量不是0.5mol,故D错误;
故选B.
B、依据乙醇燃烧生成二氧化碳和水的反应定量关系计算电子转移,1mol乙醇在O2中完全燃烧,C2H6O+3O2→2CO2+3H2O,电子转移数目为12NA,故B正确;
C、苯分子中无碳碳双键,故C错误;
D、标准状况己烷不是气体,11.2L的己烷物质的量不是0.5mol,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的分析判断,主要是气体摩尔体积条件应用分析,物质结构判断,氧化还原反应电子转移计算,掌握基础是关键,题目较简单.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
能证明Al的金属性比Mg弱的实验事实是( )
| A、Al的导电性比Mg强 |
| B、Al的原子半径比Mg小 |
| C、Al(OH)3能溶于NaOH溶液,而Mg(OH)2则不能 |
| D、Mg(OH)2的溶解性比Al(OH)3的溶解性略大 |
下列各组物质中,属于同系物的是( )
| A、CH2=CH-COOH,CH3-CH2-CH2-COOH |
| B、乙烷,2,2,3,3-四甲基丁烷 |
C、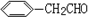 ,CH3CH2CHO ,CH3CH2CHO |
D、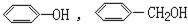 |
由乙烯推测丙烯(CH3CH=CH2)的结构或性质正确的是( )
| A、分子中3个碳原子在同一直线上 |
| B、分子中所有原子在同一平面上 |
| C、能发生加聚反应 |
| D、与氯化氢加成只生成一种产物 |
设NA为阿伏伽德罗常数的值,下列有关说法不正确的是( )
| A、标准状况下,48g O3含有的氧原子数为3NA |
| B、1mol OH-离子中含电子数目为10NA |
| C、0.5L 0.2mol?L-1的NaCl溶液中含有的Na+数是0.1NA |
| D、常温常压下,33.6L CO中含有的原子数是3NA |
下列各组物质的性质比较,正确的是( )
| A、碱性:KOH>Ca(OH)2>NaOH |
| B、氢化物稳定性:NH3>H2O>HF |
| C、酸性:HClO>H2SO4>H3PO4 |
| D、氧化性:F2<Cl2<Br2<I2 |
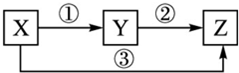
在物质分类中常存在包含关系如图B包含A,下列关系中前者包含后者.其中错误的是( )
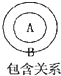

| A、有机物烃 | B、烃脂肪烃 |
| C、脂肪烃烯烃 | D、烯烃氯乙烯 |
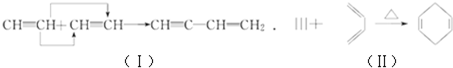
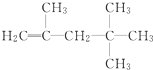 可由(填结构简式)
可由(填结构简式)