题目内容
能证明Al的金属性比Mg弱的实验事实是( )
| A、Al的导电性比Mg强 |
| B、Al的原子半径比Mg小 |
| C、Al(OH)3能溶于NaOH溶液,而Mg(OH)2则不能 |
| D、Mg(OH)2的溶解性比Al(OH)3的溶解性略大 |
考点:金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:金属性强弱判断方法有:金属之间的置换反应、金属元素氧化物的水化物碱性强弱、金属与水或酸置换出氢元素的难易程度,据此分析解答.
解答:
解:金属的金属性越强,金属与酸或水置换出氢气越容易,能置换出较不活泼的金属,金属的氧化物的水化物碱性越强,与金属的导电性强弱、原子半径、氢氧化物的溶解性无关,Al(OH)3能溶于NaOH溶液,而Mg(OH)2则不能,说明氢氧化铝的碱性小于氢氧化镁,则说明Mg的金属性大于Al,
故选C.
故选C.
点评:本题考查了金属性强弱的判断,明确金属性强弱判断方法是解本题关键,注意:金属的金属性强弱与金属失电子难易程度有关,与失电子多少无关,为易错点.

练习册系列答案
相关题目
阿司匹林是日常生活中应用广泛的医药之一.它可由下列方法合成: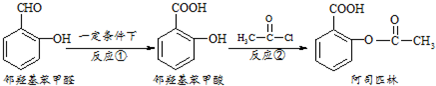
下列说法正确的是( )

下列说法正确的是( )
| A、邻羟基苯甲醇分子中所有的原子不可能在同一平面 |
| B、用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① |
| C、反应②中加入适量的NaHCO3可提高阿司匹林的产率 |
| D、与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有2种 |
结合下列各物质的性质,判断其固态属于原子晶体的是( )
| A、碳化铝,黄色晶体,熔点2200℃,熔融态不导电 |
| B、溴化铝,无色晶体,熔点98℃,熔融态不导电 |
| C、五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、氯仿、丙酮中 |
| D、溴化钾,无色晶体,熔融态时或溶于水中都能导电 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、1mol甲基(-CH3)中含有电子的数目为10NA |
| B、1mol乙醇在O2中完全燃烧,电子转移数目为12NA |
| C、1mol苯乙烯中含有的C=C数为4NA |
| D、标准状况下,11.2L的己烷所含的分子数为0.5NA |
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀.图是一种氢氧燃料电池驱动LED发光的装置.下列有关叙述正确的是( )


| A、a处通入氧气 |
| B、b处为电池正极,发生了还原反应 |
| C、该装置中只涉及两种形式的能量转化 |
| D、P-型半导体连接的是电池负极 |
下列离子反应方程式正确的是( )
| A、乙酸与CaCO3反应:2H++CO32-═CO2↑+H2O | ||
| B、苯酚与NaOH溶液反应:H++OH-═H2O | ||
| C、溴乙烷中滴入AgNO3溶液:Br-+Ag+═AgBr↓ | ||
D、乙醛与银氨溶液反应:CH3CHO+2[Ag(NH3)2-]+2OH-
|
 利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池,请填写下列空白:
利用生活中或实验室中常用的物品,根据氧化还原反应知识和电学知识,自己动手设计一个原电池,请填写下列空白: