题目内容
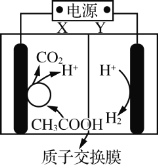
【题目】锌电池是一种极具前景的电化学储能装置。![]() 扣式可充电电池组成示意图如下。
扣式可充电电池组成示意图如下。![]() 可以在
可以在![]() 晶体中可逆地嵌入和脱除,总反应为
晶体中可逆地嵌入和脱除,总反应为![]() 。下列说法错误的是( )
。下列说法错误的是( )
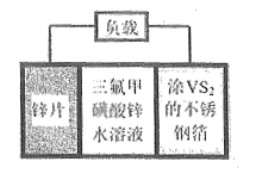
A. 放电时不锈钢箔为正极,发生还原反应
B. 放电时负极的反应为![]()
C. 充电时电池正极上的反应为:![]()
D. 充电时锌片与电源的负极相连
【答案】C
【解析】
如图:对VS2/Zn扣式可充电电池组成分析,放电时,不锈钢箔为正极,锌片为负极,电极反应Zn-2e-═Zn2+;充电时原电池的正极与外电源正极相连,作阳极,失电子发生氧化反应,原电池负极与电源负极相连,作阴极,得到电子发生还原反应。
A.放电时,不锈钢箔为正极,发生还原反应,故A正确;
B.放电时,负极为锌,锌电极反应为:Zn-2e-═Zn2+,故B正确;
C.充电时,原电池的正极接电源的正极,作阳极,失去电子,发生氧化反应,故C错误;
D.充电时,原电池负极锌片与电源的负极相连,作阴极,故D正确;
故选:C。

【题目】某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
已知:①氯化钙可与乙醇形成CaCl2·6C2H5OH
②有关有机物的沸点:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
③2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
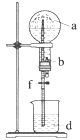
I.制备过程: 装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液。
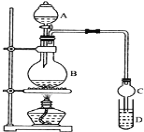
(1)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是________(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(2)球形干燥管的主要作用是_________________________。
(3)饱和Na2CO3溶液的作用是_______________________________________________________
II.提纯方法:①将D中混合液进行分离。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物。
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯。
(4)第①步分离混合液时,选用的主要玻璃仪器的名称是_________________。
(5)第②步中用饱和食盐水洗去碳酸钠后、再用饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的__________________,______________。
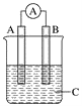
【题目】在如图所示的装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体d呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是
a(干燥气体) | b(液体) |
| |
A | NO | 水 | |
B | CO2 | 饱和NaHCO3溶液 | |
C | Cl2 | 饱和NaCl溶液 | |
D | NH3 | 1 mol·L-1盐酸 |
A.AB.BC.CD.D