题目内容
6.某同学设计了如图所示的实验装置分别测定生成的SO2气体、SO3气体的质量和O2气体的体积,此设计有4处不合理之处.请说明理由:①饱和的NaHSO3溶液改为U形管,并浸在冰水中,使SO3液化、结晶;②浓硫酸改为氢氧化钠溶液,目的是吸收SO2;③NaOH溶液改为澄清石灰水,目的是验证SO2是否完全被吸收;④伸入量筒内的导管太长,目的防止倒吸.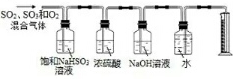
分析 SO3气体易液化,可以用冰水混合物冷却,SO2气体用碱液吸收,氧气用排水法测量,据此分析.
解答 解:如图所示的实验装置分别测定生成的SO2气体、SO3气体的质量和O2气体的体积,SO3气体的熔点为16.8℃,用冰水混合物冷却会结晶,SO2气体用碱液吸收,后面加一个澄清石灰水来检验二氧化硫是否被完全吸收,氧气用排水法测量,伸入量筒内的导管不能太长防止发生倒吸;则此设计不合理之处为:①改为U形管,并浸在冰水中,是SO3液化;②改为氢氧化钠溶液,目的是吸收SO2;③改为澄清石灰水,目的是验证SO2是否完全被吸收;④伸入量筒内的导管太长;目的防止倒吸.;
故答案为:①饱和的NaHSO3溶液改为U形管,并浸在冰水中,使SO3液化、结晶;②浓硫酸改为氢氧化钠溶液,目的是吸收SO2;③NaOH溶液改为澄清石灰水,目的是验证SO2是否完全被吸收;④伸入量筒内的导管太长,目的防止倒吸.
点评 本题考查了气体性质、检验,题目难度不大,侧重于考查学生的分析能力和对基础知识的应用能力,注意把握二氧化硫和三氧化硫的性质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O═CH3COOH+4H+.下列有关说法正确的是( )
| A. | 检测时,电解质溶液中的H+向负极移动 | |
| B. | 若有0.4mol电子转移,则在标准状况下消耗4.48 L氧气 | |
| C. | 电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O | |
| D. | 正极上发生的反应为O2+4e-+2H2O═4OH- |
1.X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-离子具有相同的电子层结构.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 单质沸点:X>Y>Z | ||
| C. | 离子半径:X2->Y+>Z- | D. | 原子半径:Y>X>Z |
18.下列关于CO2和SiO2性质的说法中,不正确的是( )
| A. | SiO2与CaCl2溶液不反应,而CO2通入CaCl2溶液中可得到白色沉淀 | |
| B. | CO2通入到水玻璃中可以得到硅酸 | |
| C. | CO2与SiO2在物理性质上差别很大 | |
| D. | CO2和SiO2都是酸性氧化物,都能与NaOH溶液反应 |
16.(1)反应N2O4(g)?2NO2(g);△H>0的平衡体系中,在298K时,平衡常数为K1,在273K时,平衡常数为K2,在373K时平衡常数为K3,K1、K2、K3之间的数量大小关系是K3>K1>K2..
(2)在298K时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
20~40s内用N2O4表示的平均反应速率为0.002mol•L-1•s-1;298K时该反应的平衡转化率=75%;反应进行至100s后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”);
(3)298K时,反应2NO2(g)?N2O4(g);△H<0达到平衡后,根据下列图象判断引起平衡移动的因素及平衡移动的方向:
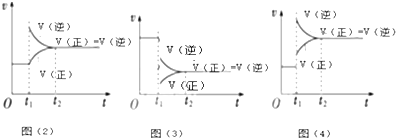
图(2)平衡将向正反应方向移动;图(3)引起平衡移动的因素是减小压强,图(4)引起平衡移动的因素是升高温度.
(2)在298K时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(3)298K时,反应2NO2(g)?N2O4(g);△H<0达到平衡后,根据下列图象判断引起平衡移动的因素及平衡移动的方向:

图(2)平衡将向正反应方向移动;图(3)引起平衡移动的因素是减小压强,图(4)引起平衡移动的因素是升高温度.