题目内容
(9分)甲、乙、丙是分别由H、C、O、Si、Al、Cu等六种元素中的两种或多种元素组成的化合物。已知甲、乙、丙均不含结晶水,含化合物甲的矿物是工业上电解法冶炼某种常见金属单质的原料,经检测甲是一种高熔点化合物,能溶于强酸、强碱溶液;化合物乙是光导纤维的主要成分;化合物丙为一种呈深蓝色的碱式盐,将34.6g丙隔绝空气加热分解生成24g黑色固体X、无色酸性气体Y(标准状况下,密度为1.96 g/L)和水。生成的Y折合成标准状况下的体积为4.48L。固体X难溶于水,能溶于硫酸,形成蓝色溶液。
请回答下列问题:
(1)写出气体Y的结构式 ,化合物丙的化学式 。
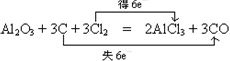
(2)写出甲与NaOH溶液反应的离子方程式 。另外,工业上常用甲与焦炭、氯气共热生成化合物丁和CO,而丁仅由两种元素组成,请写出该反应的化学方程式并标出电子转移的方向和数目 。
(3)乙溶于氢氟酸后生成一种极强的二元酸和水。经分析该酸由3种元素组成,其中氟元素的质量分数为79.17%。请写出乙溶于氢氟酸的离子方程式 。
(4)将固体X溶于适量的硫酸,往所得溶液中滴加NaOH浓溶液时,先出现蓝色絮状沉淀,继续滴加NaOH浓溶液并不断振荡,则沉淀消失形成蓝色溶液。综合以上信息可以说明蓝色絮状沉淀物具有__________性(填化学性质)。
请回答下列问题:
(1)写出气体Y的结构式 ,化合物丙的化学式 。
(2)写出甲与NaOH溶液反应的离子方程式 。另外,工业上常用甲与焦炭、氯气共热生成化合物丁和CO,而丁仅由两种元素组成,请写出该反应的化学方程式并标出电子转移的方向和数目 。
(3)乙溶于氢氟酸后生成一种极强的二元酸和水。经分析该酸由3种元素组成,其中氟元素的质量分数为79.17%。请写出乙溶于氢氟酸的离子方程式 。
(4)将固体X溶于适量的硫酸,往所得溶液中滴加NaOH浓溶液时,先出现蓝色絮状沉淀,继续滴加NaOH浓溶液并不断振荡,则沉淀消失形成蓝色溶液。综合以上信息可以说明蓝色絮状沉淀物具有__________性(填化学性质)。
(1)O="C=O" (1分) Cu3(CO3)2(OH)2 或2CuCO3·Cu(OH)2 (1分)
(2)Al2O3+2OH—=2AlO2—+H2O(2分)
 (2分)
(2分)
(3)SiO2+6HF = 2H+ + SiF62—+2H2O (2分)
(4)两性(1分)
(2)Al2O3+2OH—=2AlO2—+H2O(2分)
 (2分)
(2分)(3)SiO2+6HF = 2H+ + SiF62—+2H2O (2分)
(4)两性(1分)
甲是一种高熔点化合物,能溶于强酸、强碱溶液,说明是两性化合物,即甲是氧化铝。光导纤维的主要成分是SiO2,乙是SiO2。标准状况下,密度为1.96 g/L,所以其摩尔质量是1.96 g/L×22.4L/mol=44g/mol,显然Y是CO2,物质的量是0.2mol。固体X难溶于水,能溶于硫酸,形成蓝色溶液,说明是铜的化合物,应为X是黑色的,所以是氧化铜,物质的量是0.3mol。因为分解生成的水是34.6g-24g-8.8g=1.8g,其物质的量是0.1mol,所以丙中Cu2+、OH-、CO32-的物质的量之比是3︰2︰2,即丙的化学式为Cu3(CO3)2(OH)2 或2CuCO3·Cu(OH)2。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
