题目内容
13.(1)有①${\;}_{0}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O ②H2、D2、T2 ③石墨、金刚石 ④${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H四组微粒或物质,互为同位素的是①④(填编号,下同).互为同素异形体的是③.(2)在${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、40K、40Ca、14N、14C中共有5种元素,7种原子,中子数最多的是40K.
分析 (1)有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;相同元素组成,不同形态的单质互为同素异形体;
(2)元素的种类由质子数决定,原子符号左下角为质子数,左上角的数字为质量数,质子数和中子数只要其一不相同就属于不同核素;
解答 解:(1)解:①168O、178O和188O质子数相同,中子数不同,故互为同位素;
②H2、D2、T2 是由氢的同位素原子构成的氢分子,既不是同位素,也不是同素异形体;
③石墨、金刚石都是由碳元素形成的不同单质,互为同素异形体;
④${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H质子数相同,中子数不同,故互为同位素;
所以互为同位素的是:①④,互为同素异形体的是:③,
故答案为:①④;③;
(2)在${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H为氢元素,40K为钾元素,40Ca为钙元素,14N为氮元素、14C为碳元素,共五种元素,质子数和中子数只要其一不相同就属于不同核素,共有7种原子;原子符号左上角的数字为质量数,40K中子数为21、40Ca中子数为20、,中子数最多的是40K,
故答案为:5;7;40K.
点评 本题考查同位素、同素异形体的概念,题目难度不大,注意对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.

练习册系列答案
相关题目
3.香柠檬酚具有抗氧化功能,它的结构如图,下列说法正确的是( )
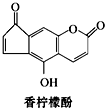

| A. | 它的分子式为C13H9O4 | |
| B. | 它与H2发生加成反应,1 mol最多可消耗7 mol H2 | |
| C. | 它与溴水发生反应,1 mol最多消耗3 mol Br2 | |
| D. | 它与NaOH溶液反应,1 mol最多消耗2 mol NaOH |
4.可逆反应:A+B?C,在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是( )
| A. | △H>0、△S>0 | B. | △H<0、△S<0 | C. | △H<0、△S>0 | D. | △H>0、△S<0 |
1.下列所描述的二氧化硫的一些化学性质中,体现二氧化硫作为还原剂的是( )
| A. | 通入溴水溶液使溴水褪色 | B. | 通入品红溶液中,使品红褪色 | ||
| C. | 溶于水形成不稳定的亚硫酸 | D. | 与碱液反应生成亚硫酸盐 |
8.下列关于化学反应限度的说法中不正确的是( )
| A. | 当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度 | |
| B. | 当一个可逆反应达到平衡状态时,各组分浓度不变,v(正)=v(逆)=0 | |
| C. | 任何可逆反应的进程都有一定的限度,只是不同的反应限度不同 | |
| D. | 化学反应的限度可以通过改变条件而改变 |
18.下列事实不能说明氯元素比硫元素非金属性强的是( )
| A. | Cl2能与H2S反应生成S | |
| B. | 溶于水时HCl是强酸,H2S是弱酸 | |
| C. | 受热时H2S能分解,HCl则不能 | |
| D. | Cl2与铁反应生成FeCl3,而S与铁反应生成FeS |
5.下列说法正确的是( )
| A. | 植物油不能使溴的四氯化碳溶液褪色( ) | |
| B. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型不同 | |
| C. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| D. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
7.下列说法正确的是( )
| A. | 质子数相同的微粒,它们的化学性质基本相同 | |
| B. | 任何原子的原子核都是由质子和中子构成 | |
| C. | L层上的电子数为奇数的元素一定是主族元素 | |
| D. | 目前使用的长式元素周期表中,最长的周期含36种元素 |