��Ŀ����
��֪����Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g�� ƽ�ⳣ��ΪK1
��Ӧ��Fe��s��+H2O��g��?FeO��s��+H2��g�� ƽ�ⳣ��ΪK2
��Ӧ��H2��g��+CO2��g��?H2O��g��+CO��g�� ƽ�ⳣ��ΪK3
����ڲ�ͬ�¶��£�K1��K2ֵ�����
��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol��L-1���ﵽƽ��ʱCO2ת����Ϊ ��
��2����Ӧ�ڵ��ʱ��H 0���������=����
��3��700�淴Ӧ�ڴﵽƽ�⣬ʹ�ø�ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ�� ������ţ�
A����С��Ӧ����� B������ˮ���� C�������¶ȵ�900��D��ʹ�ú��ʵĴ���
��4������ͼ����Ϸ�Ӧ�ٵ��� ������ţ���ͼ��v�����ʡ���Ϊ�������CO������TΪ�¶ȣ�

��5��900����з�Ӧ��H2��g��+CO2��g��?H2O��g��+CO��g������ƽ�ⳣ��K3����ֵΪ
��6�����������Ȼ�ѧ����ʽ������д��C��s��ȼ���ȵ��Ȼ�ѧ����ʽΪ�� ��
C��s��+H2O��l��=CO��g��+H2��g����H1=+175.3kJ?mol-1
2CO��g��+O2��g��=2CO2��g����H2=-566.0kJ?mol-1
2H2��g��+O2��g��=2H2O��l����H3=-571.6kJ?mol-1��
��Ӧ��Fe��s��+H2O��g��?FeO��s��+H2��g�� ƽ�ⳣ��ΪK2
��Ӧ��H2��g��+CO2��g��?H2O��g��+CO��g�� ƽ�ⳣ��ΪK3
����ڲ�ͬ�¶��£�K1��K2ֵ�����
| �¶�/�� | K1 | K2 |
| 500 | 1.00 | 3.15 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
��2����Ӧ�ڵ��ʱ��H
��3��700�淴Ӧ�ڴﵽƽ�⣬ʹ�ø�ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ��
A����С��Ӧ����� B������ˮ���� C�������¶ȵ�900��D��ʹ�ú��ʵĴ���
��4������ͼ����Ϸ�Ӧ�ٵ���

��5��900����з�Ӧ��H2��g��+CO2��g��?H2O��g��+CO��g������ƽ�ⳣ��K3����ֵΪ
��6�����������Ȼ�ѧ����ʽ������д��C��s��ȼ���ȵ��Ȼ�ѧ����ʽΪ��
C��s��+H2O��l��=CO��g��+H2��g����H1=+175.3kJ?mol-1
2CO��g��+O2��g��=2CO2��g����H2=-566.0kJ?mol-1
2H2��g��+O2��g��=2H2O��l����H3=-571.6kJ?mol-1��
���㣺��ѧƽ��ļ���,�ø�˹���ɽ����йط�Ӧ�ȵļ���,��ѧƽ���Ӱ������
ר�⣺�����������������
��������1��Fe��s��+CO2��g���TFeO��s��+CO��g��ƽ�ⳣ��ΪK1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol?L-1����ƽ��ʱCO��Ũ��Ϊcmol/L����������ʽ��c��ʾ��ƽ��ʱ���ɷֵ�Ũ�ȣ��ٸ���ƽ�ⳣ���з��̼��㣻
��2������ƽ�ⳣ�����¶ȱ仯�ж�ƽ���ƶ���������Ӧ�����仯���ɱ������ݿ�֪�����ڷ�Ӧ�ڣ��¶�Խ��ƽ�ⳣ����С��˵�������¶�ƽ�����淴Ӧ�ƶ����淴Ӧ�����Ƿ��ȷ�Ӧ������Ӧ�����ȷ�Ӧ��
��3��700�淴Ӧ�ڴﵽƽ�⣬ʹ�ø�ƽ�������ƶ������ݷ�Ӧ������ƽ���ƶ�ԭ�������жϣ�
��4��A����ͼ��֪�������¶ȣ�ƽ��������Ӧ�ƶ�����ͼ���ʾ����Ӧ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
B����ͼ��֪����ߵ㵽��ƽ�⣬�¶����ߣ��������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
C����ͼ��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�T1����ƽ��ʱ���������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
��5�����ݷ�Ӧ�٢ڵ�ƽ�ⳣ�����㷴Ӧ�۵�ƽ�ⳣ����
��6�����ø�˹���ɿ���д��C��s��ȼ���ȵ��Ȼ�ѧ����ʽ��
��2������ƽ�ⳣ�����¶ȱ仯�ж�ƽ���ƶ���������Ӧ�����仯���ɱ������ݿ�֪�����ڷ�Ӧ�ڣ��¶�Խ��ƽ�ⳣ����С��˵�������¶�ƽ�����淴Ӧ�ƶ����淴Ӧ�����Ƿ��ȷ�Ӧ������Ӧ�����ȷ�Ӧ��
��3��700�淴Ӧ�ڴﵽƽ�⣬ʹ�ø�ƽ�������ƶ������ݷ�Ӧ������ƽ���ƶ�ԭ�������жϣ�
��4��A����ͼ��֪�������¶ȣ�ƽ��������Ӧ�ƶ�����ͼ���ʾ����Ӧ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
B����ͼ��֪����ߵ㵽��ƽ�⣬�¶����ߣ��������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
C����ͼ��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�T1����ƽ��ʱ���������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ϸ�Ӧ�ٵ���ЧӦ�жϣ�
��5�����ݷ�Ӧ�٢ڵ�ƽ�ⳣ�����㷴Ӧ�۵�ƽ�ⳣ����
��6�����ø�˹���ɿ���д��C��s��ȼ���ȵ��Ȼ�ѧ����ʽ��
���
�⣺��1����ƽ��ʱCO��Ũ��Ϊcmol/L����
�� Fe��s��+CO2��g���TFeO��s��+CO��g��
��ʼ��mol/L����2 0
�仯��mol/L����c c
ƽ�⣨mol/L����2-c c
��
=1�����c=1�����Դﵽƽ��ʱCO2ת����=
��100%=50%��
�ʴ�Ϊ��50%��
��2���ɱ������ݿ�֪�����ڷ�Ӧ�ڣ��¶�Խ��ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ���У���H��0��
�ʴ�Ϊ������
��3��700�淴Ӧ�ڴﵽƽ�⣬Fe��s��+H2O��g���TFeO��s��+H2��g��������ƽ�ⳣ����������Ӧ�Ƿ��ȷ�Ӧ��ʹ�ø�ƽ�������ƶ���
A���÷�Ӧǰ����������ʵ������䣬��С��Ӧ�������ѹǿ����ƽ�ⲻ�ƶ�����A�����ϣ�
B������ˮ������ƽ��������Ӧ�ƶ�����B���ϣ�
C���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶ȵ�900�棬ƽ�����淴Ӧ�ƶ�����C�����ϣ�
D��ʹ�ú��ʵĴ������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����D�����ϣ�
�ʴ�Ϊ��B��
��4��A����ͼ��֪�������¶ȣ�ƽ��������Ӧ�ƶ�����ͼ���ʾ����Ӧ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ������ϣ���A��ȷ��
B����ͼ��֪����ߵ㵽��ƽ�⣬�¶����ߣ��������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ�ʲ��������B����
C����ͼ��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�T1����ƽ��ʱ���������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ�ʲ��������C����
�ʴ�Ϊ��A��
��5��900����з�Ӧ��Ӧ
��Fe��s��+CO2��g���TFeO��s��+CO��g��ƽ�ⳣ��ΪK1=
��Ӧ��Fe��s��+H2O��g���TFeO��s��+H2��g��ƽ�ⳣ��ΪK2=
��H2��g��+CO2��g���TH2O��g��+CO��g������ƽ�ⳣ��K3=
=
=
=1.50��
�ʴ�Ϊ��1.50��
��6����C��s��+H2O��l��=CO��g��+H2��g����H1=+175.3kJ?mol-1
��2CO��g��+O2��g��=2CO2��g����H2=-566.0kJ?mol-1
��2H2��g��+O2��g��=2H2O��l����H3=-571.6kJ?mol-1
���ݸ�˹���ɢ�+�ڡ�
+�ۡ�
��̼ȼ���ȵ��Ȼ�ѧ����ʽ��C��s��+O2��g��=2CO2��g����H=��H1+
��H2+
��H3=-393.5 kJ?mol-1��
�ʴ�Ϊ��C��s��+O2��g��=2CO2��g����H=-393.5 kJ?mol-1��
�� Fe��s��+CO2��g���TFeO��s��+CO��g��
��ʼ��mol/L����2 0
�仯��mol/L����c c
ƽ�⣨mol/L����2-c c
��
| c |
| 2-c |
| 1mol/L |
| 2mol/L |
�ʴ�Ϊ��50%��
��2���ɱ������ݿ�֪�����ڷ�Ӧ�ڣ��¶�Խ��ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ��������¶�ƽ�������ȷ�Ӧ���У���H��0��
�ʴ�Ϊ������
��3��700�淴Ӧ�ڴﵽƽ�⣬Fe��s��+H2O��g���TFeO��s��+H2��g��������ƽ�ⳣ����������Ӧ�Ƿ��ȷ�Ӧ��ʹ�ø�ƽ�������ƶ���
A���÷�Ӧǰ����������ʵ������䣬��С��Ӧ�������ѹǿ����ƽ�ⲻ�ƶ�����A�����ϣ�
B������ˮ������ƽ��������Ӧ�ƶ�����B���ϣ�
C���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶ȵ�900�棬ƽ�����淴Ӧ�ƶ�����C�����ϣ�
D��ʹ�ú��ʵĴ������ӿ췴Ӧ���ʣ�ƽ�ⲻ�ƶ�����D�����ϣ�
�ʴ�Ϊ��B��
��4��A����ͼ��֪�������¶ȣ�ƽ��������Ӧ�ƶ�����ͼ���ʾ����Ӧ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ������ϣ���A��ȷ��
B����ͼ��֪����ߵ㵽��ƽ�⣬�¶����ߣ��������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ�ʲ��������B����
C����ͼ��֪���¶�T1�ȵ���ƽ�⣬���¶�T1��T2���¶�T1����ƽ��ʱ���������CO�ĺ������ͣ�ƽ�����淴Ӧ���У���ͼ���ʾ����ӦΪ���ȷ�Ӧ����Ӧ������Ӧ�����ȷ�Ӧ��ͼ����ʵ�ʲ��������C����
�ʴ�Ϊ��A��
��5��900����з�Ӧ��Ӧ
��Fe��s��+CO2��g���TFeO��s��+CO��g��ƽ�ⳣ��ΪK1=
| c(CO) |
| c(CO2) |
��Ӧ��Fe��s��+H2O��g���TFeO��s��+H2��g��ƽ�ⳣ��ΪK2=
| c(H2) |
| c(H2O) |
��H2��g��+CO2��g���TH2O��g��+CO��g������ƽ�ⳣ��K3=
| c(CO)c(H2O) |
| c(CO2)c(H2) |
| K1 |
| K2 |
| 2.4 |
| 1.6 |
�ʴ�Ϊ��1.50��
��6����C��s��+H2O��l��=CO��g��+H2��g����H1=+175.3kJ?mol-1
��2CO��g��+O2��g��=2CO2��g����H2=-566.0kJ?mol-1
��2H2��g��+O2��g��=2H2O��l����H3=-571.6kJ?mol-1
���ݸ�˹���ɢ�+�ڡ�
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
�ʴ�Ϊ��C��s��+O2��g��=2CO2��g����H=-393.5 kJ?mol-1��
����������Ŀ�ۺ��Խϴ��漰��Ӧ���ʼ��㡢ƽ�ⳣ������ѧƽ����㡢Ӱ�췴Ӧ�����뻯ѧƽ���ƶ������ء���˹�����뷴Ӧ�ȵļ���ȣ��Ѷ��еȣ�

��ϰ��ϵ�д�
 �㽭��У��ʦ���ϵ�д�
�㽭��У��ʦ���ϵ�д� ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д�
�����Ŀ
�ܱ�ʾ�����ӵ�������ֵ���ǣ�������
| A��23g������������ȫȼ��ʧ������Ϊ0.5NA |
| B����״���£�22.4L�������ķ����� |
| C�������£�8g���麬�й��ۼ���Ϊ2NA |
| D��1L 1mol?L-1������Һ������H+ΪNA |
���Ϲ�ȷ��2014�ꡰ����ˮ�ա������������ǡ�ˮ����Դ����Water and Energy����ˮ����ȷ��2014���ҹ��������ˮ�ա��͡��й�ˮ�ܡ������������Ϊ����ǿ�Ӻ�����������ˮ��̬�������������й�˵����������������һ������ǣ�������
| A����ѧʹ��ũҩ�����ʣ�����ˮ����Ⱦ |
| B����ҵ��ˮ�ͳ���������ˮ�辻����������ִ���ŷ� |
| C��Ϊ�˽�Լ�����ɱ����ɽ���ֽ��������������ˮԴ������ |
| D����������ˮ��Դ������ˮ��Դ��Լ�ͺͻ����Ѻ��;��� |
�е¹��������о������˹��ϳɵĵ�112��Ԫ�ص���ʽ����Ϊ��Copernicium������Ӧ��Ԫ�ط���λ��Cn������Ԫ�ص�������Ϊ�˼�������ѧ�Ҹ������������������˹��ϳ�Cn�Ĺ��̿ɱ�ʾΪ��
Zn+
Pb�T
Cn+
n������������ȷ���ǣ�������
70 30 |
208 82 |
277 112 |
1 0 |
| A�������ϳɹ��������ڻ�ѧ�仯 | ||
| B��CnԪ�ص����ԭ������Ϊ277 | ||
C��
| ||
| D��CnԪ��λ��Ԫ�����ڱ��ĵ������ڣ��Ǹ���Ԫ�� |

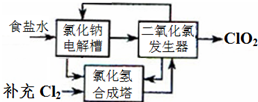 ������������Ƭ����Ч�ɷ֣�ClO2����һ�ָ�Ч����ȫ��ɱ������������
������������Ƭ����Ч�ɷ֣�ClO2����һ�ָ�Ч����ȫ��ɱ������������