��Ŀ����
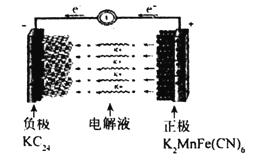
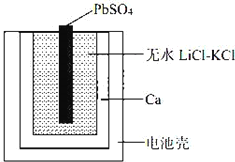
����Ŀ����ͼ��ʾ��ij��ѧ��ȤС�������һ��ȼ�ϵ�أ���̽���ȼҵԭ���ʹ�ͭ����ԭ����������װ����XΪ�����ӽ���Ĥ������Ҫ��ش��������:

��1��ͨ�������ĵ缫Ϊ_____���������������������������˵缫��ӦʽΪ_________��
��2�����缫Ϊ_______����������������������������װ���е�ⷴӦ�Ļ�ѧ����ʽΪ_________________��
��3��ij��ͭ�к������������Ͳ������ʣ�ͨ����⾫�ƺ�Ϊ�ӵ��Һ���Ƶ�����ͭ����(CuSO4��5H2O)����������¹������̣�
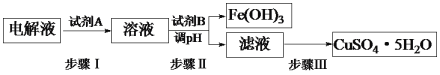
��֪�����ֽ��������ӿ�ʼ�����ͳ�����ȫ��pH��
�������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
Fe3�� | 1.9 | 3.2 |
Fe2�� | 7.6 | 9.6 |
Cu2�� | 4.7 | 6.7 |
�ٲ���I�м����Լ�A��Ŀ����_____________________________���Լ�AӦѡ��______(�����)��
a������ b���������� C�����Ը��������Һ
�ڲ���II���Լ�BΪ_________�����һ�ּ��ɣ�������pH�ķ�Χ��___________��
�۲���III�IJ����Ǽ���Ũ����___________�����ˡ�
���𰸡����� O2+4e����2H2O��4OH�� ���� 2NaCl��2H2O![]() 2NaOH��C12����H2�� ��Fe2������ΪFe3�� b CuO��Cu(OH)2��Cu2(OH)2CO3 3.2��pH<4.7 ��ȴ�ᾧ
2NaOH��C12����H2�� ��Fe2������ΪFe3�� b CuO��Cu(OH)2��Cu2(OH)2CO3 3.2��pH<4.7 ��ȴ�ᾧ
��������
��1��ȼ�ϵ����ͨ�������ĵ缫�������������ϵõ��ӷ�����ԭ��Ӧ��������ȼ��ʧ���ӷ���������Ӧ��
��2�����缫��������̼����������װ���е���Ȼ��Ʊ�����Һʱ�������������ӷŵ磻
��3�����õ�ⷨ���д�ͭ�ᴿʱ��ͭӦ����������ͭ����������֪�����Ļ��˳��ΪFe>Cu>Ag>Pt>Au������ڵ�������Ag��Pt��Au����ʧȥ���ӣ������γ������࣬˫��ˮ���������ԣ����Խ�������������Ϊ���������ӣ��Ҳ��������������ӣ�ʵ�ֹ����Һ��ķ�����õķ����ǹ��ˣ�����pHʱ�ܶȻ�С�����γɳ����������Դ˷�����
��1��ȼ�ϵ����ͨ�������������ĵ缫�������������ϵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ![]()
�ʴ�Ϊ��������![]() ��
��
��2�����缫����ԭ��ظ�����������������̼������������Ȼ��Ʊ�����Һʱ����ⷴӦ�Ļ�ѧ����ʽΪ��![]() ��
��
�ʴ�Ϊ��������![]() ��
��
��3���ٲ���I�м����Լ�A�ǹ������⣬Ŀ���ǽ�Fe2+����ΪFe3+��������������ɫ�������������������в��������ʣ���������Ⱦ
�ʴ�Ϊ����Fe2+����ΪFe3+��b��
�ڳ�ȥͭ���ӵ���Һ�е��������������ӣ�Ϊ�˲������������ӣ�����������ˮ���ԭ������ȥ�����Լ��룺CuO��Cu(OH)2��Cu2(OH)2CO3�����ݼ��ֽ��������ӿ�ʼ�����ͳ�����ȫ��pH���ݣ���Ҫ������pH��Χ��3.2��pH<4.7��
�ʴ�Ϊ��CuO��Cu(OH)2��Cu2(OH)2CO3��3.2��pH<4.7��
������ͭ��Һ�õ�����ͭ����Ĺ����ǣ�����Ũ������ȴ�ᾧ�����ˣ�
�ʴ�Ϊ����ȴ�ᾧ�����ˡ�

 ��������������������ϵ�д�
��������������������ϵ�д�����Ŀ���п�Ժһ�����³ɹ�ʵ���˼����Ч������ϩ�������ڴ����������⣬�������о����ɻ�ż����Ӧ������ϩ���䷴Ӧ���£�2CH4(g)C2H4(g)��2H2(g)����H��0
��ѧ�� | H��H | C��H | C��C | C��C |
E(kJ/mol) | a | b | c | d |
��1����֪��ػ�ѧ���ļ������ϱ��������Ʊ���ϩ��Ӧ�Ħ�H��____________ (�ú�a��b��c��d�Ĵ���ʽ��ʾ)��
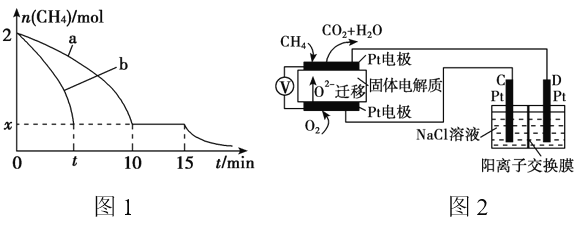
��2��T1�¶�ʱ����1 L�ĺ��ݷ�Ӧ���г���2mol CH4 ��������������Ӧ����Ӧ������ 0��15min CH4�����ʵ�����ʱ��仯��ͼ1�����10��15minʱH2��Ũ��Ϊ1.6mol/L��
��0��10min��CH4��ʾ�ķ�Ӧ����Ϊ__________mol/(L��min)��
����ͼ1������a������b�ֱ��ʾ���¶�T1ʱ��ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n(CH4)�仯���ߣ����б�ʾ����������ϴ�������� ________ (�a���� ��b��)��
��15minʱ�����ı���練Ӧ����������n(CH4)����ͼ1����ʾ�仯����ı������������_____________________________________(�δ�һ������)��
��3��ʵ����v����k��c2(CH4)��v����k��c(C2H4)��c2(H2)����k����k��Ϊ���ʳ��������¶��йأ�T1�¶�ʱk����k���ı�ֵΪ______ (����ֵ)�������¶���T1���ߵ�T2����Ӧ��������ı���v��____v��(�>����������<��)���жϵ�������_________________ ��
��4��������Ա����˼���ȼ�ϵ�ز����ڵ�⡣��ͼ2��ʾ��������Dz����� Y2O3�� ZrO2�Ĺ��壬���ڸ����´���O2����
��C����PtΪ______ ��(����������� )��
�ڸõ�ع���ʱ������Ӧ����ʽΪ_____________________��
���øõ�ص�ⱥ��ʳ��ˮ��һ��ʱ����ռ�����������������Ϊ112mL����������������Һ��25��ʱpH��_______ (������ǰ��NaCl��Һ�������Ϊ500mL)��