题目内容
【题目】下表为长式周期表的一部分,其中的编号代表对应的元素。
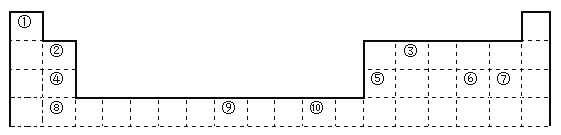
请回答下列问题:
(1)表中属于d区的元素是___________(填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为_________。
(3)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是___________(用元素符号表示)。
(4)按原子轨道的重叠方式,③与⑥形成的化合物中σ键有______个,π键有______个。
(5)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为_______;该元素与元素①形成的分子X的空间构形为___________。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:__________________。
【答案】 ⑨ 苯 Cl> S> Mg> Al 2 2 1 三角锥形 Be(OH)2+2NaOH=Na2BeO2+2H2O
【解析】(1)区的名称来自于按照构造原理最后填入电子的轨道名称,属于表中属于d区的元素是⑨;(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子是苯;(3)④ ⑤ ⑥ ⑦四种元素分别是Mg、Al、S、Cl。金属性越强第一电离能越大。但由于镁元素的3s轨道电子处于全充满状态,所以第一电离能对于Al元素的,则第一电离能由大到小的顺序是Cl> S> Mg> Al;(4)按原子轨道的重叠方式,③与⑥形成的化合物是二硫化碳,分子中含有2个双键。而双键是由1个σ键和1个π键构成的,所以分子中σ键有2个,π键有2个;(5)某元素的特征电子排布式为nsnnpn+1,则该元素是第ⅤA族元素。所以该元素原子的核外最外层电子的孤对电子数为1;该元素与元素①形成的分子X是氨气,其空间构形为三角锥形结构,属于极性分子;(6)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。由于⑤是铝元素,能氢氧化铝能和氢氧化钠溶液反应生成偏铝酸钠和水,则元素②即Be的氢氧化物与NaOH溶液反应的化学方程式Be(OH)2+2NaOH=Na2BeO2+2H2O。

 全优点练单元计划系列答案
全优点练单元计划系列答案