题目内容
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
C
解析

 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案已知N2(g)+3H2(g) 2NH3(g) △H=?92.4 kJ·mol-1,在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
2NH3(g) △H=?92.4 kJ·mol-1,在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下,下列说法正确的是
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 2 mol N2、6 mol H2 | 2 mol NH3 |
| NH3的浓度(mol·L-1) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 放出Q2 kJ | 吸收Q3 kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
C.2p1=2p3<p2 D.达到平衡时丙容器中NH3的体积分数最大
在三种不同条件下,分别向容积为2L的恒容容器中加入2molA和1molB,发生反应如下:2A(g)+B(g) 2D(g) △H=Q kJ·mol-1,相关条件和数据见下表。
2D(g) △H=Q kJ·mol-1,相关条件和数据见下表。
| | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 800 | 800 | 850 |
| 达到平衡所需时间/min | 40 | a | 30 |
| D物质平衡浓度/mol·L-1 | 0.5 | b | 0.6 |
| 反应的能量变化/ kJ | Q1 | Q2 | Q3 |
下列说法正确的是
A.当容器中气体的相对分子质量不再发生变化时,说明该反应达到平衡状态
B.如果实验Ⅱ相比实验Ⅰ使用了催化剂,则a>40, b=0.5
C.实验Ⅲ达到平衡时,向其中通入少量惰性气体,容器压强增大,平衡向右移动
D.由表中信息可知Q<0,并且有Q1 =Q2<Q3
在一密闭容器中有如下反应:aX(g)+bY(s)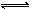 nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:( )
nW(g);ΔH=Q。某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:( )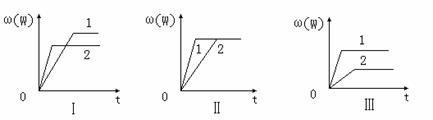
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间。其它条件不变时,下列分析正确的是( )
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a<n |
| B.图Ⅱ可能是在同温同压下催化剂对反应的影响,且2使用的催化剂效果好 |
| C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n=a+b |
| D.图Ⅲ可能是不同温度对反应的影响,且T1>T2,Q<0 |
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ(恒容)和Ⅱ(恒压)中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量与时间的变化关系如图所示,则下列有关推断正确的是( )
A.该反应的化学方程式:3X+2Y 3Z 3Z |
| B.若两容器中均达到平衡后,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所用时间小于t0 |
| C.若两容器中均达到平衡后,两容器中Z的物质的量分数相同,则Y为固态或液态 |
| D.达平衡后,若对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
在一定温度下,反应C(s)+H2O(g)  CO(g)+H2(g)达到平衡的标志是( )
CO(g)+H2(g)达到平衡的标志是( )
| A.正反应与逆反应速率均为零 |
| B.v(H2O生成)=v(CO消耗) |
| C.单位时间内反应物减少的分子数等于生成物增加的分子数 |
| D.压强不随时间的变化而变化 |
下列反应条件的控制中不恰当的是( )。
| A.为防止铁生锈,在其表面涂一层防锈油漆 |
| B.为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C.为加快KClO3的分解速率,加入MnO2 |
| D.为加快H2O2的分解速率,把反应容器放到冷水中冷却 |
反应C(s)+H2O(g)  CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )。
CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )。
①增加C的量 ②将容器的体积减小一半 ③保持体积不变,充入氮气使体系的压强增大 ④保持压强不变,充入氮气使体系的体积增大
| A.①② | B.②③ | C.①③ | D.③④ |
已知某条件下,合成氨反应的数据如下:
N2(g)+3H2(g) 2NH3(g)
2NH3(g)
起始浓度/mol·L-1 1.0 3.0 0.2
2s末浓度/mol·L-1 0.6 1.8 1.0
4s末浓度/mol·L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是( )
| A.2s末氨气的反应速率=0.4mol·(L·s)-1 |
| B.前2s时间内氨气的平均反应速率=0.4mol·(L·s)-1 |
| C.前4s时间内氨气的平均反应速率=0.3mol·(L·s)-1 |
| D.2s~4s时间内氨气的平均反应速率=0.2mol·(L·s)-1 |