题目内容
在一定温度下,反应C(s)+H2O(g)  CO(g)+H2(g)达到平衡的标志是( )
CO(g)+H2(g)达到平衡的标志是( )
| A.正反应与逆反应速率均为零 |
| B.v(H2O生成)=v(CO消耗) |
| C.单位时间内反应物减少的分子数等于生成物增加的分子数 |
| D.压强不随时间的变化而变化 |
D
解析

练习册系列答案
相关题目
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:
2X(g)+Y(g)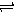 Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是( )
Z(g)△H<0,反应经60s达到平衡并生成0.3 mol Z,则下列说法中正确的是( )
| A.以Y浓度变化表示的反应速率为0.0005 mol/(L·s) |
| B.其他条件不变,将容器体积扩大至20 L,则Z的平衡浓度变为原来的1/2 |
| C.其他条件不变,将容器体积缩小至5L,平衡正向移动,平衡常数增大 |
| D.其他条件不变,升高温度逆反应速率加快,正反应速率减慢 |
在一定温度条件下,对于已达到平衡的反应:
FeCl3 +3KSCN  3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是
3KCl+Fe(SCN)3,在此溶液中作如下处理,平衡左移的是
| A.加入少量氯化钾固体 | B.加入少量氯化铁固体 |
| C.减少Fe(SCN)3的浓度 | D.加水稀释 |
下列关于催化剂的说法不正确的是( )
| A.温度越高,催化剂的催化效果越好 |
| B.汽车排气管上的“催化转化器”能减少有害气体排放 |
| C.催化剂可以改变化学反应速率,但反应前后质量和化学性质不变 |
| D.锌与盐酸反应时,加入几滴硫酸铜溶液可加快反应速率,但硫酸铜不作催化剂 |
下图是向100 mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像,根据如图所得结论正确的是 ( )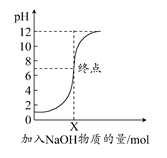
| A.原来盐酸的物质的量浓度为0.1 mol·L-1 |
| B.NaOH溶液的浓度为0.1 mol·L-1 |
| C.原来盐酸的物质的量浓度为1 mol·L-1 |
| D.NaOH溶液的浓度为0.01 mol·L-1 |
硫酸是一种重要的化工产品,2SO2+O2 2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
2SO3是生产过程中的重要反应。下列对于该反应的说法中正确的是
| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零 |
| C.如果反应前充入由18O原子组成的O2,反应达到平衡状态时,18O只存在于O2和SO3中 |
| D.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成n mol Z,同时生成2n mol Y
| A.①② | B.①④ | C.②③ | D.③④ |
下列对可逆反应的认识正确的是( )
| A.SO2+Br2+2H2O=H2SO4+2HBr与2HBr+H2SO4(浓)=Br2+SO2↑+2H2O互为可逆反应 |
| B.既能向正反应方向进行,又能向逆反应方向进行的反应叫可逆反应 |
| C.在同一条件下,同时向正、逆两个方向进行的反应叫可逆反应 |
| D.电解水生成氢气和氧气与氢气和氧气点燃生成水的反应是可逆反应 |