题目内容
10.设NA代表阿伏伽德罗常数,下列叙述正确的是( )| A. | 将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,若不考虑挥发,溶液中含有的NH4+数目小于NA | |
| B. | 24g石墨烯(单层石墨)中含有六元环的个数为NA | |
| C. | 标准状况下,6.72LNO2与足量水反应转移电子数目为0.2NA | |
| D. | 4.6gC2H6O加入足量的金属钠,充分作用,生成H2分子数一定为0.05NA |
分析 A、溶液为中性,则氢离子与氢氧根离子浓度相等,根据电荷守恒可知硝酸根离子的物质的量与铵根离子的物质的量相等;
B、依据n=$\frac{m}{M}$计算物质的量,结合石墨烯中平均每个六元环含碳原子2个;
C、0.3mol二氧化氮与水反应生成0.2mol硝酸和0.1mol一氧化氮,转移了0.2mol电子;
D、分子式为C2H6O的不一定为乙醇,甲醚的分子式也是C2H6O,但甲醚不与钠反应;
解答 解:A、将1molNH4NO3溶于一定浓度的稀氨水中,溶液呈中性,则氢离子与氢氧根离子浓度相等,根据电荷守恒,铵根离子与硝酸根离子物质的量相等,所以溶液中铵根离子的物质的量为1mol,则溶液中一定含有NA个NH4+,故A错误;
B、依据n=$\frac{m}{M}$计算物质的量=$\frac{24g}{12g/mol}$=2mol,石墨烯中平均每个六元环含碳原子2个,则2mol碳原子含有六元环的个数为NA,故B正确;
C、标准状况下,6.72L NO2的物质的量为0.3mol,0.3mol二氧化氮与水反应生成0.2mol硝酸和0.1mol一氧化氮,反应转移了0.2mol电子,转移的电子数目为0.2NA,故C正确;
D、分子式为C2H6O的有乙醇和甲醚两种异构体,乙醇与钠反应,而甲醚不与钠反应,4.6gC2H6O的物质的量为4.6g÷46g/mol═0.1mol,若全为乙醇,则产生氢气分子数一定为0.05NA,否则不是,故D错误;
故选BC.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
1.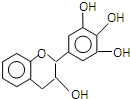 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A. | 1 molEGC与足量溴水反应可消耗2 mol Br2 | |
| B. | EGC与苯酚属于同系物 | |
| C. | 在一定条件下,EGC中的羟基可被氯原子取代生成氯代烃 | |
| D. | 1mol EGC与含1.5mol Na2CO3的水溶液恰好完全反应生成1.5molCO2 |
18.燃料电池的能量利用率比内燃机高,已应用于汽车中,如图为某燃料电池工作示意图,其中C1和C2均为多孔性纳米电极(不考虑电解质参与电极反应).下列有关说法不正确的是( )


| A. | a口放出气体为N2 | |
| B. | 电池总反应的产物与甲醇燃烧产物一样 | |
| C. | 用该电池电解精制铜,当消耗1mol甲醇时,可溶解粗铜中3mol铜 | |
| D. | 质子将由C1电极区经交换膜向C2电极区运动 |
5.如图是金属晶体的面心立方最密堆积方式的晶胞示意图,在密堆积中处于同一密层上的原子组合是( )
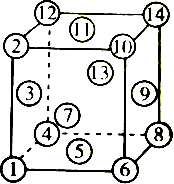

| A. | ④⑤⑥⑩⑪⑫ | B. | ②③④⑤⑥⑦ | C. | ①④⑤⑥⑧ | D. | ①②⑪⑭⑧⑤ |
13.下列有关化学与生活、工业的叙述中,不正确的是( )
| A. | 工业上生产玻璃、水泥、漂白粉及用铁矿石冶炼铁,均需要用石灰石为原料 | |
| B. | 未成熟的苹果肉遇碘酒变蓝色,成熟苹果的汁液能与银氨溶液发生反应 | |
| C. | 面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物,过氧化苯甲酰属于有机物 | |
| D. | 大力实施矿物燃料“脱硫、脱硝技术”,可以减少硫的氧化物和氮的氧化物对环境的污染. |
14.如图中表示外界条件(T、P)的变化对下列反应的影响L(s)+G(g)?2R(g);△H>0,y轴表示的是( )
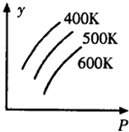

| A. | 平衡时,混合气体中R的百分含量 | B. | 平衡时,混合气中G的百分含量 | ||
| C. | G的转化率 | D. | L的转化率 |
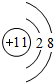 ,C的原子结构示意图是
,C的原子结构示意图是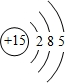 .
.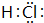 、A的氢氧化物的电子式
、A的氢氧化物的电子式 .
. .Q的离子符号为OH-.
.Q的离子符号为OH-.