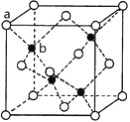
题目内容
【题目】为了缓解温室效应,科学家提出了多种回收和利用CO2的方案。
方案I:利用FeO吸收CO2获得H2
ⅰ.6FeO(s)+CO2(g)=--2Fe3O4(s)+C(s) △H1=-76.0kJ/mol
ⅱ.C(s)+2H2O(g)=CO2(g)+2H2(g) △H2=+113.4kJ/mol
(1)3FeO(s)+H2O(g)=Fe3O4(s)+H2(g) △H3=________。
(2)在反应i中,每放出38.0kJ热量,有_______gFeO被氧化。
方案II:利用CO2制备CH4
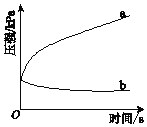
300℃时,向2L恒容密闭容器中充入2molCO2和8molH2,发生反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。
CH4(g)+2H2O(g) △H4,混合气体中CH4的浓度与反应时间的关系如图所示。
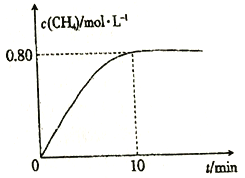
(3) ①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=_________。
②300℃时,反应的平衡常数K=____________。
③保持温度不变,向平衡后的容器中再充入2molCO2和8molH2,重新达到平衡时CH4的浓度_________(填字母)。
A.等于0.8mol/L B.等于1.6 mol/L C.0.8 mol/L <c(CH4)<1.6 mol/L D.大于1.6 mol/L
(4)300℃时,如果该容器中有1.6molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),则v正____v逆(填“>”“<”或“=”)。
(5)已知:200℃时,该反应的平衡常数K=64.8L2·mol-2。则△H4______0(填“>”“<”或“=”)。
方案Ⅲ:用碱溶液吸收CO2
利用100mL3mol/LNaOH溶液吸收4.48LCO2(标准状况),得到吸收液。
(6)该吸收液中离子浓度的大小排序为______________。将该吸收液蒸干、灼烧至恒重,所得固体的成分是__________(填化学式)。
【答案】 +18.7kJ/mol 144 0.32 mol.L-1·min-1 25L2·mol-2 D > < c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) Na2CO3
【解析】(1)已知ⅰ.6FeO(s) +CO2(g)=--2Fe3O4(s) +C(s) △H1=-76.0kJ/mol
ⅱ.C(s) +2H2O(g)=CO2(g) +2H2(g) △H2= +113.4kJ/mol
根据盖斯定律,由ⅰ×![]() +ⅱ×
+ⅱ×![]() 得反应3FeO(s) +H2O(g)=Fe3O4(s) +H2(g) △H3=△H1×
得反应3FeO(s) +H2O(g)=Fe3O4(s) +H2(g) △H3=△H1×![]() +△H2×
+△H2×![]() =-76.0kJ/mol×
=-76.0kJ/mol×![]() +113.4kJ/mol×
+113.4kJ/mol×![]() =+18.7kJ/mol;(2)在反应i6FeO(s) +CO2(g)=--2Fe3O4(s) +C(s) △H1=-76.0kJ/mol中,每放出38.0kJ热量,有3mol FeO 参与反应,而其中有
=+18.7kJ/mol;(2)在反应i6FeO(s) +CO2(g)=--2Fe3O4(s) +C(s) △H1=-76.0kJ/mol中,每放出38.0kJ热量,有3mol FeO 参与反应,而其中有![]() 的FeO中的铁元素由+2价变为+3价,故被氧化的 FeO的质量为:3mol×
的FeO中的铁元素由+2价变为+3价,故被氧化的 FeO的质量为:3mol×![]() ×72g/mol=144g;
×72g/mol=144g;
(3) CO2(g) +4H2(g)![]() CH4(g) +2H2O(g)
CH4(g) +2H2O(g)
起始浓度(mol/L) 1 4 0 0
改变浓度(mol/L) 0.8 3.2 0.8 1.6
平衡浓度(mol/L) 0.2 0.8 0.8 1.6
①从反应开始到恰好达到平衡时,H2 的平均反应速率v(H2) =![]() =0.32 mol.L-1·min-1;②300℃时,反应的平衡常数K=
=0.32 mol.L-1·min-1;②300℃时,反应的平衡常数K= =
=![]() =25L2·mol-2;③保持温度不变,向平衡后的容器中再充入2 molCO2和8 molH2,则物质的量增大2倍,若平衡不移动则平衡后CH4 的浓度应该是原来的2倍即1.6 mol/L,但在恒容情况下增大两倍投料,相当于增大压强,平衡向气体缩小的正反应方向移动, CH4 的浓度增大,大于1.6 mol/L,答案选D;(4)300℃时,如果该容器中有1.6 molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),Qc=
=25L2·mol-2;③保持温度不变,向平衡后的容器中再充入2 molCO2和8 molH2,则物质的量增大2倍,若平衡不移动则平衡后CH4 的浓度应该是原来的2倍即1.6 mol/L,但在恒容情况下增大两倍投料,相当于增大压强,平衡向气体缩小的正反应方向移动, CH4 的浓度增大,大于1.6 mol/L,答案选D;(4)300℃时,如果该容器中有1.6 molCO2、2.0molH2、5.6molCH4、4.0molH2O(g),Qc=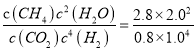 =14则反应未达平衡,向正反应方向进行,v正> v逆;(5)已知: 300℃时,反应的平衡常数K=25L2·mol-2;200℃时,该反应的平衡常数K=64.8L2·mol-2。则降低温度,K值增大,平衡向正反应方向移动,正反应为放热反应,△H4<0;(6)实验室中常用NaOH溶液来进行洗气和提纯,当100mL 3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液为等浓度的碳酸钠和碳酸氢钠的混合液,水解显碱性,且碳酸根的水解程度大于碳酸氢根,各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);将该吸收液蒸干、灼烧至恒重,由于碳酸氢钠受热分解,故所得固体的成分是Na2CO3。
=14则反应未达平衡,向正反应方向进行,v正> v逆;(5)已知: 300℃时,反应的平衡常数K=25L2·mol-2;200℃时,该反应的平衡常数K=64.8L2·mol-2。则降低温度,K值增大,平衡向正反应方向移动,正反应为放热反应,△H4<0;(6)实验室中常用NaOH溶液来进行洗气和提纯,当100mL 3mol/L的NaOH溶液吸收标准状况下4.48LCO2时,所得溶液为等浓度的碳酸钠和碳酸氢钠的混合液,水解显碱性,且碳酸根的水解程度大于碳酸氢根,各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);将该吸收液蒸干、灼烧至恒重,由于碳酸氢钠受热分解,故所得固体的成分是Na2CO3。

 同步练习强化拓展系列答案
同步练习强化拓展系列答案【题目】工业上采用氯化铵焙烧菱锰矿制备高纯度碳酸锰,工艺流程如下:
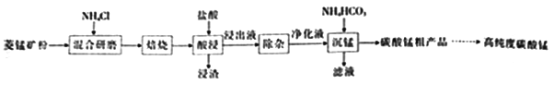
己知相关信息如下:
①菱猛矿的主要成分是MnCO3,还含少量Fe、Al、Ca、Mg等元素。
②氢氧化物沉淀的条件:Al3+、Fe3+完全沉淀的pH分别为4.7、3 2;Mn2+、Mg2+开始沉淀的pH分别为8.1、9.1。
③“焙烧”过程的主要反应MnCO3+2NH4Cl=MnCl2+2NH3↑+CO2↑+H2O。
④常温下,几种难溶物的Ksp如下表所示:
难溶物 | Mn(OH)2 | MnCO3 | CaF2 | MgF2 |
Ksp | 2.0×10-13 | 2.0×10-11 | 2.0×10-10 | 7.0×10-11 |
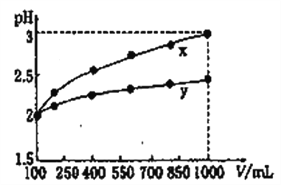
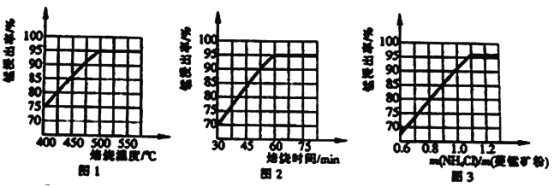
(1)分析图1、图2、图3,最佳的焙烧温度、焙烧时间、m(NH4Cl)/m(美锰矿粉)分别为____、____、____。
(2) “除杂”过程如下:
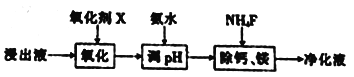
①已知几种氧化剂氧化能力的强弱顺序为(NH4)2S2O3>H2O2 >Cl 2>MnO2 >Fe2+,则氧化剂X宜选择_________(填字母)。
A. (NH4)2S2O3 B. MnO2 C. H2O2 D. Cl 2
②调节pH时,pH 可取的最低值为_____________。
③当CaF2、MgF2两种沉淀共存时,若溶液中c(Ca2+)=1.0×10-3mol/L,则c(Mg2+)=____mol/L。
(3)“沉锰”过程中,不用碳酸纳溶液替代NH4HCO3溶液,可能的原因是__________。
(4)测定碳酸锰粗产品的纯度。实验步骤:
①称取0.5000g碳酸锰粗产品于300mL锥形瓶中,加少量水湿润,再加25mL磷酸,移到通风橱内加热至240℃,停止加热,立即加入2 g硝酸铵,保温,充分反应后,粗产品中的碳酸锰全部转化为[Mn(PO4)2]3-,多余的硝酸铵全部分解。用氮气赶尽锥形瓶内的氮氧化物,冷却至室温。
②将上述锥形瓶中的溶液加水稀释至100mL,滴加2-3滴指示剂,然后用浓度为0.2000mol/L的硫酸亚铁铵[(NH4)Fe(SO4)2]标准溶液滴定,发生的反应为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO43-。到达滴定终点时,消耗的硫酸亚铁铵标准溶液的体积为20.00mL。
计算:碳酸锰粗产品的纯度=___________。
误差分析:若滴定终点时发现滴定管尖嘴处产生了气泡,则测得的碳酸锰粗产品的纯度_____(填“偏高”“偏低”或 “无影响”)。