题目内容
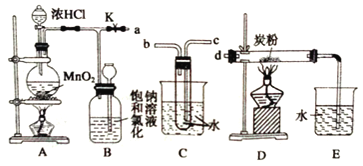
【题目】为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
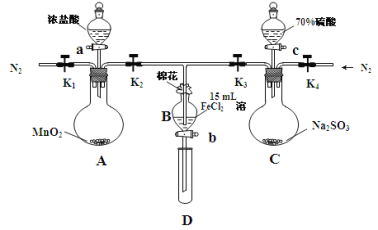
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是_______________________________________________。
(2)棉花中浸润的溶液化学式为_________________________。
(3)A中发生反应的化学方程式为____________________________________。
(4)过程Ⅳ中检验其中Fe3+ 和Fe2+的试剂分别为___________和__________。
确定有Fe3+ 和Fe2+现象分别是_______________和____________________。
(5)过程Ⅵ,检验B溶液中是否含有SO42—的操作是_____________________。
(6)甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:
过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
甲 | 有Fe3+无Fe2+ | 有SO |
乙 | 既有Fe3+又有Fe2+ | 有SO |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |
Cl2 > Fe3+ > SO2的是________(填“甲”“乙”“丙”)。
【答案】排除装置中的空气,防止干扰 NaOH溶液MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2H2O硫氰化钾铁氰化钾溶液变红出现蓝色沉淀向D试管中加入适量盐酸,再加BaCl2溶液,若有白色沉淀产生,说明溶液中含有SO42—乙、丙
MnCl2 + Cl2↑+ 2H2O硫氰化钾铁氰化钾溶液变红出现蓝色沉淀向D试管中加入适量盐酸,再加BaCl2溶液,若有白色沉淀产生,说明溶液中含有SO42—乙、丙
【解析】
试题(1)空气中的氧气也能氧化亚铁离子为铁离子,所以通入氮气的目的是排除装置中的空气,防止干扰;
(2)氯气有毒,不能排放到空气中污染空气,所以用沾有NaOH溶液的棉花堵塞T型导管,防止氯气逸出;
(3)A装置是制取氯气的反应,化学方程式为MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2H2O;
MnCl2 + Cl2↑+ 2H2O;
(4)根据离子的特征反应,过程Ⅳ中检验其中Fe3+和Fe2+的试剂分别为硫氰化钾和铁氰化钾,铁离子遇硫氰化钾溶液变红,亚铁离子遇铁氰化钾生成蓝色沉淀;
(5)D试管中可能含有亚硫酸根离子,所以检验硫酸根离子需除去亚硫酸根离子,具体操作为向D试管中加入适量盐酸,再加BaCl2溶液,若有白色沉淀产生,说明溶液中含有SO42-;
(6)甲的结论:IV中B溶液含有铁离子说明氧化性Cl2 > Fe3+ ,VI中B溶液含有硫酸根离子,若B溶液中氯气有剩余,则氯气会氧化二氧化硫生成硫酸根离子,不能判断氧化性Fe3+ > SO2;乙的结论:IV中B溶液含有Fe3+和Fe2+,说明氧化性Cl2 > Fe3+ 且氯气不足,所以VI中B溶液含有硫酸根离子,则一定是Fe3+氧化二氧化硫为硫酸根离子,所以判断氧化性Fe3+ > SO2,因此可得氧化性Cl2 > Fe3+ > SO2的结论;丙的结论:IV中B溶液含有铁离子说明氧化性Cl2 > Fe3+ ,VI中B溶液含有Fe2+,若是氯气氧化二氧化硫,不会有Fe2+生成,说明铁离子与二氧化硫发生氧化还原反应,Fe3+被还原为Fe2+,所以氧化性Fe3+ > SO2,因此可得氧化性Cl2 > Fe3+ > SO2的结论,所以能够证明氧化性: Cl2 > Fe3+ > SO2的是乙、丙。