题目内容
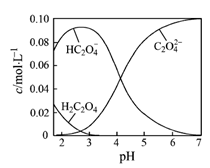
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4–)+ c(C2O42–)=0.100 mol·L–1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是
A.pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)>c(HC2O4–)
B.c(Na+)=0.100 mol·L–1的溶液中:c(H+)+c(H2C2O4)=c(OH–)+c(C2O42–)
C.c(HC2O4–)=c(C2O42–)的溶液中:c(Na+)>0.100 mol·L–1+c(HC2O4–)
D.pH=7的溶液中:c(Na+)<2c(C2O42–)
【答案】B
【解析】
试题分析:A、根据图像知pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)<c(HC2O4–),错误;B、根据物料守恒和电荷守恒分析c(Na+)=0.100 mol·L-1的溶液中:c(H+) + c(H2C2O4) = c(OH–) + c(C2O42–),正确;C、c(HC2O4–) = c(C2O42–)的溶液中:c(Na+) > 0.100 mol·L–1 + c(HC2O4–) ,错误;D、由图像知PH=7的溶液为草酸钠溶液,草酸根水解,c(Na+) > 2c(C2O42–),错误。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目