题目内容
2.下列说法正确的是( )| A. | 在实验室中将工业酒精转化为无水酒精的方法是:加入过量的生石灰后分液 | |
| B. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| C. | 用重结晶法提纯NaCl和KNO3混合物中的KNO3 | |
| D. | 用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈酸性 |
分析 A、根据生石灰的性质分析,生石灰和水能反应;
B、苯是通过煤的干馏得到的;
C、KNO3的溶解度随温度变化很大,NaCl的溶解度温度变化不大;
D、酸溶液稀释pH变大.
解答 解:A、在工业酒精中加入生石灰后蒸馏可制得无水酒精,故A错误;
B、苯是通过煤的干馏得到的,故B错误;
C、KNO3的溶解度随温度变化很大,故可用用重结晶法提纯NaCl和KNO3混合物中的KNO3,故C正确;
D、用湿润的pH试纸测定溶液的pH,测定结果偏小,该溶液一定呈碱性,故D错误;
故选C.
点评 本题考查较综合,涉及有机物的结构与性质、物质的提纯、pH的测定等,注重基础知识的考查,选项B为易错点,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
12.下列有关原电池的说法中不正确的是( )
| A. | 任何氧化还原反应原则上都可以设计成原电池 | |
| B. | 原电池中电子从负极经导线流入正极 | |
| C. | 原电池中正极得电子数与负极失电子数一定相等 | |
| D. | 铜-锌-稀硫酸组成的原电池,电解质溶液中H+向负极移动 |
13.质量相同的铝粉和足量的盐酸、足量的NaOH溶液完全反应,在同温同压下生成气体的体积比是( )
| A. | 1:2 | B. | 2:1 | C. | 1:1 | D. | 1:4 |
10.下列措施对增大反应速率明显有效的是( )
| A. | Al在氧气中燃烧生成Al2O3,将Al粉改为Al片 | |
| B. | Fe与稀盐酸反应制取H2时,加入少量醋酸钠粉末 | |
| C. | Na与水反应时增大钠的用量 | |
| D. | 灼热的碳与水蒸气反应时,向体系中通入水蒸气 |
17.银锌钮扣电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为Ag2O+Zn$?_{充电}^{放电}$2Ag+ZnO,在此电池放电时,则下列说法正确的是( )
| A. | 氧化银为正极,被氧化 | |
| B. | 负极发生的反应为:Zn+2OH--2e-═ZnO+H2O | |
| C. | Zn为负极,被还原 | |
| D. | 该装置中的电解质为酸性物质 |
7.下列各项表达式正确的是( )
| A. | N2的电子式: | B. | F-的结构示意图: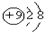 | ||
| C. | 二氧化碳分子的结构式为 O-C-O | D. | NaCl的电子式: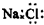 |
14.现有部分短周期元素的性质或原子结构如表:下列叙述正确的是( )
| 元素代号 | 元素性质或原子结构 |
| T | M层上的电子数为6个 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7 |
| A. | 元素X的一种同位素可测定文物年代,这种同位素的符号是12C | |
| B. | 元素Z的非金属性比元素T弱 | |
| C. | Y和T位于同一主族 | |
| D. | T、X、Y、Z四种元素的最高价氧化物水化物中化学性质明显不同于其它三种的是碳酸 |
11.下列变化中,不需要破坏化学键的是( )
| A. | 氯化氢溶于水 | B. | 氯化铵受热分解 | C. | 干冰升华 | D. | 氯化钠熔化 |
12.下列除杂的有关操作和试剂均正确的是( )
| 组别 | 被提纯物质 | 杂质 | 除杂试剂 | 除杂操作 |
| A | CO2 | SO2 | Na2CO3溶液 | 洗气 |
| B | 乙酸乙酯 | 乙酸 | 乙醇和浓H2SO4 | 加热 |
| C | 乙烷 | 乙烯 | 溴水、碱石灰 | 洗气 |
| D | 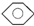 | CH3CH2OH | H2O | 分液 |
| A. | A | B. | B | C. | C | D. | D |