题目内容
【题目】NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A. 标准状况下,5.6L 一氧化氮和5.6L 氧气混合后的分子总数为0.5NA
B. 等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1
C. 一定温度下,1L 0.50 mol/L NH4Cl溶液与2L 0.25 mol/L NH4Cl溶液含NH4+的物质的量不同
D. 标准状况下,等体积的N2和CO所含的原子数均为2NA
【答案】C
【解析】
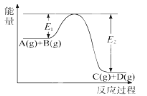
A.5.6L一氧化氮和5.6L 氧气混合后发生反应2NO+O2=2NO2,2NO2![]() N2O4,反应为气体分子数减少的反应,因此混合后的分子总数小于0.5NA,故A错误;
N2O4,反应为气体分子数减少的反应,因此混合后的分子总数小于0.5NA,故A错误;
B.磷酸为弱酸,不可完全电离出H+,故B错误;
C. NH4+水解,浓度不同,水解程度不同,因此1L 0.50 mol/L NH4Cl溶液与2L 0.25 mol/L NH4Cl溶液含NH4+的物质的量不同,故C正确;
D.标准状况下,等体积的N2和CO物质的量相等,所含的原子数相等,但不一定为2NA,故D错误;
答案:C

【题目】某化学小组想制取CuO并证明CuO能加快KClO3的分解速率,设计并进行如下实验:
(一)制取CuO
①称取2 g胆矾研细后放入烧杯,加适量蒸馏水溶解;
②向步骤①所得溶液中逐滴加入NaOH溶液至铜离子沉淀完全;
③将步骤②所得沉淀过滤、洗涤,灼烧至恒重,研细备用。
回答下列问题:
(1)上述实验步骤中溶解、过滤时玻璃棒的作用依次是_____________。
(2)步骤③中灼烧前后,沉淀颜色的变化为_______。
(3)利用化学方法证明铜离子已经沉淀完全的操作是____________。
(二)证明CuO能加快KClO3的分解速率,并与MnO2的催化效率进行比较
用下图装置进行实验,且均以生成相同状况下20 mL氧气为准,其它可能影响实验的因素均已忽略,相关数据见下表:

实验序号 | KClO3质量 | 其它物质质量 | 待测数据 |
① | 1.5 g | 无其他物质 | |
② | 1.5 g | CuO 0.5 g | |
③ | 1.5 g | MnO2 0.5 g |
(4)上述实验中的待测数据指_____________;该实验除以上思路外,还可以通过测定______________来比较CuO和MnO2的催化效率。
(5)本实验装置图中量气装置由乳胶管和仪器A_______________(填名称)及50 mL___________(填“酸式”或“碱式”)滴定管改造后组装而成;
(6)为探究CuO在实验②中是否起催化作用,需补做如下实验:
a.CuO的质量有没有改变;
b.CuO的化学性质有没有改变。
简述验证CuO质量是否改变的操作过程_________________________。