题目内容
【题目】回答下列问题:
(1)已知某链状烷烃分子中电子数为42。则:
①该烷烃的分子式为________________,该烷烃分子的所有同分异构体的结构简式为________________。
②上述同分异构体中,在相同条件下沸点最低的是________________(写结构简式)。
(2)分子式为CaH20的链状烷烃中a为________,分子式为C8Hb的链状烷烃中b为________,与CO2密度(同温同压下)相同的烷烃的分子式为________。若上述三种烃各为1mol,分别在足量O2中燃烧,消耗O2最多的是________(填具体分子式)。
【答案】![]()
![]() 、
、![]() 、
、![]()
![]() 9 18
9 18 ![]()
![]()
【解析】
(1)根据烷烃通式进行分析,结构碳原子数和碳架中支键的数目对沸点的影响进行分析;
(2)根据烃的通式及分子组成、烃燃烧耗氧的计算进行分析。
(1)烷烃分子的通式为![]() ,则其分子中电子数为
,则其分子中电子数为![]() ,解得
,解得![]() ,故该烷烃的分子式为
,故该烷烃的分子式为![]() ;烷烃
;烷烃![]() 有三种同分异构体,其结构简式分别为
有三种同分异构体,其结构简式分别为![]() 、
、![]() 、
、![]() ;烷烃分子中,碳原子数相同时,所带支链越多,其沸点越低,因此烷烃
;烷烃分子中,碳原子数相同时,所带支链越多,其沸点越低,因此烷烃![]() 三种同分异构体中,
三种同分异构体中,![]() 沸点最低;
沸点最低;
(2)根据烷烃通式![]() ,可求出
,可求出![]() 为9,
为9,![]() 为18;同温同压下,密度与
为18;同温同压下,密度与![]() 相同的烷烃的相对分子质量为44,由
相同的烷烃的相对分子质量为44,由![]() 可求出
可求出![]() 为3,即该烷烃的分子式为
为3,即该烷烃的分子式为![]() ;若同为
;若同为![]() 烃(
烃(![]() ),消耗
),消耗![]() 的多少取决于
的多少取决于![]() 的大小,
的大小,![]() 的值越大,消耗
的值越大,消耗![]() 越多,此题中消耗
越多,此题中消耗![]() 最多的是
最多的是![]() 。
。

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
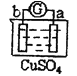
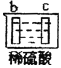
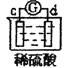
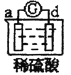
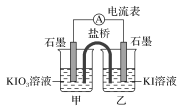
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c