题目内容
【题目】在1L定容的密闭容器中,可以证明可逆反应N2+3H2![]() 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是
A. c(N2):c(H2):c(NH3)=1:3:2
B. 一个N≡N 断裂的同时,有3个H-H生成
C. 其他条件不变时,混合气体的密度不再改变
D. v正(N2)═2 v逆(NH3)
【答案】B
【解析】试题分析:A、当各物质的浓度之比符合化学计量数之比时不一定是平衡状态,A错误;B、断裂1个N≡N代表正反应速率,同时有3个H—H生成,代表逆反应速率,且符合化学计量数之比,证明已达化学平衡状态,B正确;C、在定容的容器中,气体的质量不变,体积不变,所以气体的密度一直不变,不能判断化学平衡是否到达,C错误;D、逆反应氨气的反应速率是正反应氮气的反应速率的2倍,D错误,答案选B。

【题目】正丁醚常用作有机反应的溶剂.实验室制备正丁醚的反应和主要实验装置如下:2CH3CH2CH2CH2OH ![]() (CH3CH2CH2CH2)2O+H2O
(CH3CH2CH2CH2)2O+H2O
反应物和产物的相关数据如下
相对分子质量 | 沸点/℃ | 密度/(gcm﹣3) | 水中溶解性 | |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 几乎不溶 |
合成反应:
①将6mL浓硫酸和37g正丁醇,按一定顺序添加到A中,并加几粒沸石.
②加热A中反应液,迅速升温至135℃,维持反应一段时间.分离提纯.
③待A中液体冷却后将其缓慢倒人盛有70mL水的分液谝斗中,振摇后静置,分液得粗产物.
④粗产物依次用40mL水、20mL NaOH溶液和40mL水洗涤,分液后加入约3g无水氯化钙颗粒,静置一段时间后弃去氯化钙.
⑤将上述处理过的粗产物进行蒸馏,收集馏分,得纯净正丁醚11g.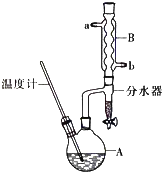
请回答:
(1)步骤①中浓硫酸和正丁醇的添加顺序为 .
(2)加热A前,需先从(填“a”或“b”)口向B中通入水.
(3)步骤③的目的是初步洗去 , 振摇后静置,粗产物应从分液漏斗的(填“上”或“下”)口分离出.
(4)步骤③巾最后一次水洗的目的为 .
(5)步骤⑤中,加热蒸馏时应收集(填选项字母)左右的馏分.a.100℃b.117℃c. 135℃d.142℃
(6)反应过程中会观察到分水器中收集到液体物质,且分为上下两层,随着反应的进行,分水器中液体逐渐增多至充满时,上层液体会从左侧支管自动流回A.分水器中上层液体的主要成分为 , 下层液体的主要成分为 .
(7)本实验中,正丁醚的产率为 .

