题目内容
【题目】请按要求作答:
(1)请根据官能团的不同对下列有机物进行分类:
①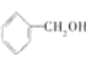 ②
②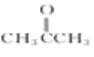 ③
③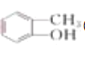 ④
④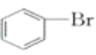 ⑤
⑤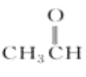 ⑥
⑥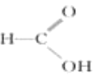 ⑦
⑦![]()
Ⅰ.醇: ________酮: ________醛: ________(填序号);
Ⅱ.④的官能团的名称为 ________,⑦的官能团的名称为 ________;
(2)分子式为 C4H8且属于烯烃的有机物的同分异构体有 ________种;
(3) ![]() 的名称为: ________;写出
的名称为: ________;写出![]() 聚合生成高分子化合物的化学方程式 ________;
聚合生成高分子化合物的化学方程式 ________;
(4) 键线式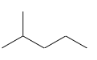 表示的有机物名称为 ________;与其互为同分异构体且一氯代物有两种的烃的结构简式________;
表示的有机物名称为 ________;与其互为同分异构体且一氯代物有两种的烃的结构简式________;
(5)篮烷分子的结构如图所示:![]()
①篮烷的分子式为: ________,其二氯代物有 ________种;
②若使 1mol 该烃的所有氢原子全部被氯原子取代,需要 ________mol 氯气。
(6)某烷烃碳架结构如图所示:![]() ,此烷烃的一溴代物有 ________种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 ________,名称为 ________;
,此烷烃的一溴代物有 ________种;若此烷烃为炔烃加氢制得,则此炔烃的结构简式为 ________,名称为 ________;
【答案】① ② ⑤ 溴原子 酯基 3 苯乙烯 ![]() 2-甲基戊烷
2-甲基戊烷 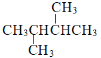 C10H12 19 12 6
C10H12 19 12 6 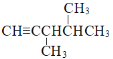 3,4-二甲基-1-戊炔
3,4-二甲基-1-戊炔
【解析】
(1)分别写出各物质的官能团和属于哪类物质。
(2)按照烯烃书写规则写出分子式为C4H8且属于烯烃的有机物的同分异构体。
(3)苯乙烯![]() 聚合生成高分子化合物聚苯乙烯。
聚合生成高分子化合物聚苯乙烯。
(4)键线式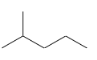 表示的有机物为(CH3)2CHCH2CH2CH3,与其互为同分异构体且一氯代物有两种的烃,即烃有两种位置的氢。
表示的有机物为(CH3)2CHCH2CH2CH3,与其互为同分异构体且一氯代物有两种的烃,即烃有两种位置的氢。
(5)①篮烷的二氯代物结构按照氯原子的位置分别进行书写;②烃与氯气发生取代反应,取代一个氢原子消耗1个氯气。
(6)某烷烃碳架结构如图所示:![]() ,此烷烃有6种位置的氢,若此烷烃为炔烃加氢制得,即碳碳之间是碳碳三键,根据碳只有四个价键,因此碳碳三键只可能在从左到右的1、2号碳原子上。
,此烷烃有6种位置的氢,若此烷烃为炔烃加氢制得,即碳碳之间是碳碳三键,根据碳只有四个价键,因此碳碳三键只可能在从左到右的1、2号碳原子上。
(1)①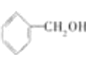 含有醇羟基,属于醇;②
含有醇羟基,属于醇;②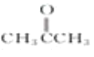 含有羰基,属于酮;③
含有羰基,属于酮;③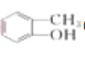 含有酚羟基,属于酚;④
含有酚羟基,属于酚;④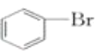 含有卤素原子,属于卤代烃;⑤
含有卤素原子,属于卤代烃;⑤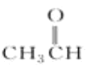 ,含有醛基,属于醛;⑥
,含有醛基,属于醛;⑥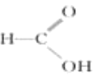 含有羧基,属于羧酸;⑦
含有羧基,属于羧酸;⑦![]() 含有酯基,属于酯。
含有酯基,属于酯。
Ⅰ.根据前面分析得到醇为①;酮为②;醛为⑤;故答案为:①;②;⑤。
Ⅱ.④的官能团的名称为溴原子,⑦的官能团的名称为酯基;故答案为:溴原子;酯基。
(2)分子式为C4H8且属于烯烃的有机物的同分异构体有CH2=CHCH2CH3、CH2=C(CH3)CH3、CH3CH=CHCH3共3种;故答案为:3。
(3)![]() 的名称为:苯乙烯;
的名称为:苯乙烯;![]() 聚合生成高分子化合物的化学方程式
聚合生成高分子化合物的化学方程式
![]() ;故答案为:苯乙烯;
;故答案为:苯乙烯;![]() 。
。
(4)键线式 表示的有机物为(CH3)2CHCH2CH2CH3,名称2-甲基戊烷;与其互为同分异构体且一氯代物有两种的烃,即烃有两种位置的氢,其结构简式
表示的有机物为(CH3)2CHCH2CH2CH3,名称2-甲基戊烷;与其互为同分异构体且一氯代物有两种的烃,即烃有两种位置的氢,其结构简式 ;故答案为:2-甲基戊烷;
;故答案为:2-甲基戊烷;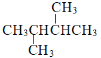 。
。
(5)①篮烷的分子式为:C10H12,其二氯代物结构为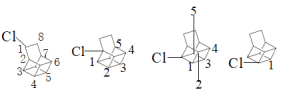 ,共19种;故答案为:C10H12;19。
,共19种;故答案为:C10H12;19。
②烃与氯气发生取代反应,取代一个氢原子消耗1个氯气,因此若使1mol该烃的所有氢原子全部被氯原子取代,需要12mol氯气;故答案为:12。
(6)某烷烃碳架结构如图所示:![]() ,此烷烃有6种位置的氢,因此一溴代物有6种;若此烷烃为炔烃加氢制得,即碳碳之间是碳碳三键,根据碳只有四个价键,因此碳碳三键只可能再从左到右的1、2号碳原子上,此炔烃的结构简式为
,此烷烃有6种位置的氢,因此一溴代物有6种;若此烷烃为炔烃加氢制得,即碳碳之间是碳碳三键,根据碳只有四个价键,因此碳碳三键只可能再从左到右的1、2号碳原子上,此炔烃的结构简式为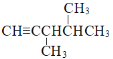 ,名称为3,4-二甲基-1-戊炔;故答案为:6;
,名称为3,4-二甲基-1-戊炔;故答案为:6;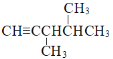 ;3,4-二甲基-1-戊炔。
;3,4-二甲基-1-戊炔。

【题目】观察下列模型并结合有关信息,判断下列说法不正确的是( )
晶体硼(其每个结构单元中有12个B原子) | NaCl | S8 | HCN | |
结构模型示意图 |
|
|
|
|
备注 | 熔点2573K | —— | 易溶于CS2 | —— |
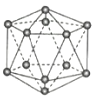
A.晶体硼属于原子晶体,结构单元中含有30个B-B键,含20个正三角形
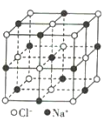
B.NaCl晶体中每个Na+周围距离最近且相等的Na+有6个
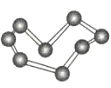
C.S8分子中的共价键为非极性键
D.HCN分子中含有2个σ键,2个π键
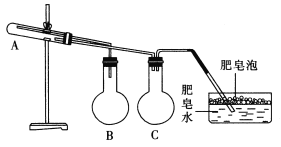
【题目】实验室用 CH3CH2OH 分两步制备 1,2-二溴乙烷。现用少量的溴和足量的乙醇制备 1,2-二溴乙烷的装置如图所示:
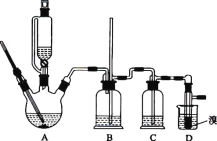
有关数据列表如下:
物质名称 | 乙醇 | 1,2-二溴乙烷 | 乙醚 |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g·cm -3) | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)装置A 中发生的化学方程式为 ________,反应类型为 ________,在此制备实验中,要尽可能迅速地把反应温度提高到 170 ℃左右,其最主要目的是 ________________(填字母)。
a.引发反应 b.防止乙醇挥发 c.减少副产物乙醚生成 d.加快反应速率
(2)装置B 的作用是 ________,在装置C 中应加入 ________(填字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(3)装置D 中实验现象为 ________。
(4)将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 ________(填“上”或“下”)层。
(5)反应过程中应用冷水冷却装置 D,其主要目的是 ________________;不用冰水原因 ________。
(6)若制得的产物中混有乙醚,得到纯净的产物的操作是________。
【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。请你结合下列有关图示和所学知识回答:
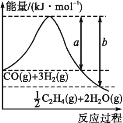
(1)用CO2催化加氢可以制取乙烯:CO2(g)+3H2(g)![]() C2H4(g)+2H2O(g)。若该反应体系的能量随反应过程变化关系如图所示,则该反应的ΔH=___(用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的ΔH=-152kJ·mol-1,则表中的x=___。
C2H4(g)+2H2O(g)。若该反应体系的能量随反应过程变化关系如图所示,则该反应的ΔH=___(用含a、b的式子表示)。又知:相关化学键的键能如下表所示,实验测得上述反应的ΔH=-152kJ·mol-1,则表中的x=___。
化学键 | C=O | H—H | C=C | C—H | H—O |
键能/kJ·mol-1 | 803 | 436 | x | 414 | 464 |
(2)键能是将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。已知下列化学键的键能如下表:
化学键 | N≡N | O | N—N | N—H | O—H |
946 | 497 | 193 | 391 | 463 |
写出1mol气态肼(H2N—NH2)燃烧生成氮气和水蒸气的热化学方程式:___。
(3)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。
①科学家提出由CO2制取C的太阳能工艺如图所示。
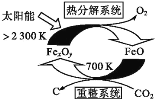
若“重整系统”发生的反应中![]() =6,则FexOy的化学式为___。“热分解系统”中每分解1molFexOy,转移电子的物质的量为___。
=6,则FexOy的化学式为___。“热分解系统”中每分解1molFexOy,转移电子的物质的量为___。
②工业上用CO2和H2反应合成二甲醚。已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1,CH3OCH3(g)+H2O(g)=2CH3OH(g) ΔH2=+23.4kJ·mol-1,则2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH3=___kJ·mol-1。
CH3OCH3(g)+3H2O(g) ΔH3=___kJ·mol-1。