��Ŀ����
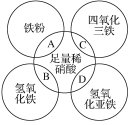
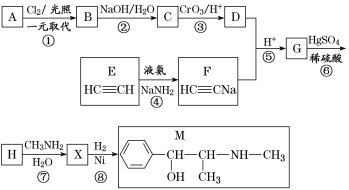
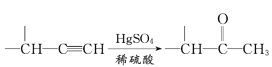
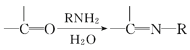
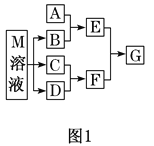
����Ŀ��ij����ѧϰС����ճ������в���ȱ�ٵĵ�ζƷM����̽������֪C����D��ȼ�շ�����ɫ���档M���������ʵ�ת����ϵ��ͼ1��ʾ(���ֲ�������ȥ)��
(1)д��B�ĵ���ʽ________��
(2)��A��һ�ַǽ������ʣ��ҿ���������뵼����ϣ�д��A��Bˮ��Һ��Ӧ�����ӷ���ʽ__________________________��
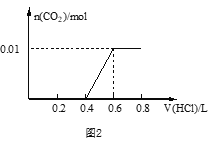
(3)��A��CO2���壬A��B��Һ�ܹ���Ӧ����Ӧ�����õ���Һ�������ᷴӦ�����ɵ�CO2���ʵ������������������ͼ2��ʾ����A��B��Һ��Ӧ����Һ���������ʵĻ�ѧʽΪ_____________��c(HCl)=________mol/L��
(4)��A��һ�ֳ����������ʣ���A��B��Һ�ܹ���Ӧ��������F��Һ��μ���E��Һ���ӱ�����������ʵ��������______________________________________��
(5)��A��һ�ֿ����������ʵĻ�����, A��B��Ӧ����������E��E��F��E��D������ð���̣�������E��D�ķ�Ӧ��������D�Ĺܵ��Ƿ�й¶��д��E��D��Ӧ�Ļ�ѧ����ʽΪ___________________��
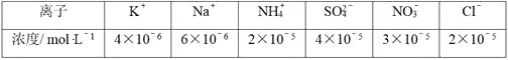
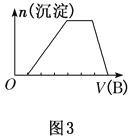
(6)��A��һ����Һ�����ܺ���H����NH![]() ��Mg2����Fe3����Al3����CO32-��SO42-�е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ3��ʾ���ɴ˿�֪������Һ�п϶����е�������_____________________�����ǵ����ʵ���Ũ��֮��Ϊ______________��
��Mg2����Fe3����Al3����CO32-��SO42-�е�ijЩ���ӣ��������Һ�м���B��Һʱ�������ɳ��������ʵ�����B��Һ����������仯��ͼ3��ʾ���ɴ˿�֪������Һ�п϶����е�������_____________________�����ǵ����ʵ���Ũ��֮��Ϊ______________��
���𰸡�![]() Si+2OH- +2H2O=SiO32-+2H2�� NaOH��Na2CO3 0.05 ���а�ɫ�������ɣ�����������������ʧ 3Cl2��8NH3===N2��6NH4Cl H����Al3����
Si+2OH- +2H2O=SiO32-+2H2�� NaOH��Na2CO3 0.05 ���а�ɫ�������ɣ�����������������ʧ 3Cl2��8NH3===N2��6NH4Cl H����Al3����![]() ��
��![]() c(H��)��c(Al3��)��c(
c(H��)��c(Al3��)��c(![]() )��c(
)��c(![]() )��1��1��2��3
)��1��1��2��3
��������
(1) C����D��ȼ�շ�����ɫ���棬Ϊ������������Ӧ����HCl������֪CΪH2��DΪCl2��FΪHCl��M���ճ������в���ȱ�ٵĵ�ζƷ����ת����ϵ��֪��M����Һ�������������������B������֪MΪNaCl��BΪNaOH��
(2)��A��һ�ַǽ������ʣ��ҿ���������뵼����ϣ���AΪSi��Si��NaOH��ˮ��Һ��Ӧ����Na2SiO3��H2��
(3) �����У���0.4L��0.6L������ӦNaHCO3+HCl=NaCl+CO2��+H2O���ý���������Ϊ200mL������ʼ����������̼ʱ��������Ϊ400mL������200mL��������Һ�е����ʳɷ�NaOH��Na2CO3��
(4) ��A��һ�ֳ����������ʣ�����NaOH��Һ�ܹ���Ӧ����AΪAl��EΪNaAlO2��������HCl��Һ��μ���NaAlO2��Һ�У������������������������������ܽ⣻
(5) ��A��һ�ֵ��ʣ�ʵ���ҿ���A��NaOH��Ӧ��ȡ����E����EΪNH3��AΪ��Σ�E������������ð���̣�������E�������ķ�Ӧ�������������Ĺܵ��Ƿ�й¶��������������Ӧ�����Ȼ�泥�ͬʱ���ɵ�����
(6) ��ͼ��֪����ʼ����NaOHû�г����������������һ����H+��һ��û��CO32-�������г��������������ʧ����һ��û��Mg2+��Fe3+��һ������Al3+���м�γ������������䣬ӦΪNH4++OH-=NH3H2O�ķ�Ӧ������NH4+���ɵ���غ��֪һ������SO42-�����ݸ������ĵ�NaOH���������ӷ���ʽ����n(H+)��n(Al3+)��n(NH4+)֮�ȣ��ٽ�ϵ���غ������n(SO42-)�ı�����ϵ���ݴ˼��㡣
(1)BΪNaOH�������ʽΪ![]() ��
��
(2) AΪSi��Si��NaOH��ˮ��Һ��Ӧ����Na2SiO3��H2����Ӧ�����ӷ���ʽΪSi+2OH- +2H2O=SiO32-+2H2����
(3) �����У���0.4L��0.6L������ӦNaHCO3+HCl=NaCl+CO2��+H2O���ý���������Ϊ200mL������ʼ����������̼ʱ��������Ϊ400mL������200mL��������Һ�е����ʳɷ�NaOH��Na2CO3������0.01molCO2��Ҫ������Ϊ200mL����Ϸ�Ӧԭ��NaHCO3+HCl=NaCl+CO2��+H2O����c(HCl)=![]() =0.05mol/L��
=0.05mol/L��
(4) ��A��һ�ֳ����������ʣ�����NaOH��Һ�ܹ���Ӧ����AΪAl��EΪNaAlO2��������HCl��Һ��μ���NaAlO2��Һ�У������������������������������ܽ⣬�ʿ���������Ϊ��Һ�����а�ɫ��״�������ɣ��Ҳ��ϵ����ӣ����������ܽ�������ʧ��
(5) ��A��һ�ֵ��ʣ�ʵ���ҿ���A��NaOH��Ӧ��ȡ����E����EΪNH3��AΪ��Σ�E������������ð���̣�������E�������ķ�Ӧ�������������Ĺܵ��Ƿ�й¶��������������Ӧ�����Ȼ�泥�ͬʱ���ɵ�������Ӧ����ʽΪ��3Cl2+8NH3=N2+6NH4Cl��
(6) ��ͼ��֪����ʼ����NaOHû�г����������������һ����H+��һ��û��CO32-�������г��������������ʧ����һ��û��Mg2+��Fe3+��һ������Al3+���м�γ������������䣬ӦΪNH4++OH-=NH3H2O�ķ�Ӧ������NH4+���ɵ���غ��֪һ������SO42-��������ӦH++OH-=H2O������������NaOH��Һ�����Ϊ1�����������ӦAl3++3OH-=Al(OH)3��������������NaOH��Һ�����Ϊ3�����������ӦNH4++OH-=NH3H2O��笠�������������Ϊ2�������n(H+)��n(Al3+)��n(NH4+)=1��1��2���ɵ���غ��֪��n(H+)��n(Al3+)��n(NH4+)��n(SO42-)=1��1��2��3����c(H+)��c(Al3+)��c(NH4+)��c(SO42-)=1��1��2��3��

 �ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�
�ǻۿ����ܾ�100�ֵ�Ԫ���ؼ��ϵ�д�