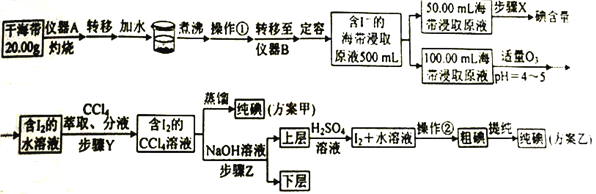
题目内容
【题目】如图,隔板K可左右移动,甲中充入2 mol A和1 mol B,乙中充入2mol C和1mol He,此时K 停在0处,发生反应2A(g)+B(g)![]() 2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是( )
2C(g),达到平衡后,恢复至温度。下列有关说法不正确的是( )
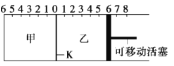
A.达平衡后,K最终停留在左侧刻度0~2之间
B.若平衡时K在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
【答案】B
【解析】
试题分析:A.2A(g)+B(g)2C(g),由于甲中充入2 mol A和1 mol B,反应向正反应方向移动,A中压强降低,最多能转化为2 mol C,但是由于反应是可逆反应,所以C的物质的量在0-2 mol之间,所以达到平衡后,隔板K不再滑动,最终停留在左侧刻度0-2之间,故A正确;B.“隔板K最终停留在左侧1处”说明反应后气体体积为5格,即物质量为2.5mol,甲中气体的物质的量为2.5 mol,乙中A、B、C三种气体的总量比甲中至少多1 mol,即大于3.5 mol,故乙中气体的体积要在6刻度右侧,故B错误;C.隔板可以滑动,说明是等压条件.乙中充入1molHe,等于给甲加压,平衡右移,B的物质的量减小,则甲容器中B的物质的量小于乙容器中B的物质的量,故C正确;D.平衡移动,气体体积会发生变化,隔板随之滑动,当隔板不移动时,说明达到平衡状态,故D正确。故选B。

 名校课堂系列答案
名校课堂系列答案【题目】T℃时,将A和B各0.32 mol充入恒容密闭容器中,发生反应:A(g)+B(g)![]() 2C(g) △H=-a kJ·mol-1 (a>0),反应过程中测定的数据如下表,下列说法正确的是( )
2C(g) △H=-a kJ·mol-1 (a>0),反应过程中测定的数据如下表,下列说法正确的是( )
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ
B.恒温, 如果压缩容器体积,B的浓度和体积分数均不变
C.若起始时向容器中充入 0.64 mol A 和 0.64 mol B, 则达平衡时 n(C)<0.40 mol
D.恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大
【题目】X、Y、Z、W、R是元素周期表前四周期中的常见元素,其相关信息如下表:
元素 | 相关信息 |
X | 组成蛋白质的基础元素,其最高正化合价与最低负化合价的代数和为2 |
Y | 地壳中含量最高的元素 |
Z | 存在质量数为23,中子数为12的核素 |
W | 生活中大量使用其合金制品,工业上可用电解熔融氧化物的方法制备其单质 |
R | 有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)R在元素周期表中的位置为______;X、Z、W三种元素的原子半径从大到小的顺序是________(用元素符号表示)。
(2)X与氢两元素按原子数目比1∶3和2∶4构成分子A和B,A的催化氧化方程式为_______;B的结构式为_______;化合物Z2Y中存在的化学键类型为________。
(3)W溶于Z的最高价氧化物的水化物的离子方程式_______________。
(4)用RCl3溶液腐蚀铜线路板的离子方程式为______。检验溶液中R3+常用的试剂是________,可以观察到的现象是________________。