题目内容
【题目】综合利用CO2对环境保护及能源开发意义重大。
(1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是____。
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
(2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃时,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行放出CO2,Li4SiO4再生,说明该原理的化学方程式是____________________________________________。
(3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。
反应A:CO2+H2O ![]() CO+H2+O2
CO+H2+O2
已知:
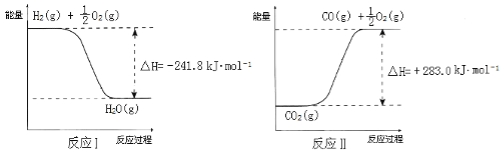
则反应A的热化学方程式是___________________________________________________。
(4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下:

① 电极b发生 (填“氧化”或“还原”)反应。
② CO2在电极a放电的反应式是___________________________。
【答案】(1) a b(2分) (2)CO2 + Li4SiO4![]() Li2CO3 + Li2SiO3(2分)
Li2CO3 + Li2SiO3(2分)
(3) CO2(g) + H2O(g) = CO(g) + H2(g) +O2(g) ΔH = +524.8 kJ·mol-1 (2分)
(4)① 氧化(2分) ② CO2 + 2e- = CO + O2- (2分)
【解析】
试题(1)由于CO2是酸性氧化物,所以如果要寻找吸收CO2的其他物质,应该在可在碱性氧化物中寻找或者可在ⅠA、ⅡA族元素形成的氧化物中寻找,答案选ab。
(2)根据题意该原理的化学方程式是CO2 + Li4SiO4![]() Li2CO3 + Li2SiO3。
Li2CO3 + Li2SiO3。
(3)根据盖斯定律可知将反应Ⅱ的热化学方程式减去反应Ⅰ的热化学方程式,整理可得反应A的热化学方程式是CO2(g)+H2O(g)=CO(g)+H2(g)+O2(g) ΔH=+524.8KJ/mol;
(4)①根据装置图可知电极b氧离子失去电阻转化为氧气,则发生氧化反应。
②电极a有CO生成,这说明CO2得到电子生成CO和氧离子,则CO2在电极a放电的反应式是CO2 + 2e- = CO + O2-。

 快捷英语周周练系列答案
快捷英语周周练系列答案