题目内容
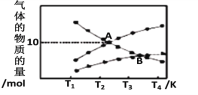
【题目】在容积一定的密闭容器中,可逆反应A(g)+B(g)![]() xC(g),有下图所示的关系曲线,根据下图下列判断正确的是
xC(g),有下图所示的关系曲线,根据下图下列判断正确的是

A.p3>p4,y轴表示A的转化率
B.p3>p4,y轴表示混合气体的密度
C.p3<p4,y轴表示B的质量分数
D.p3<p4,y轴表示混合气体的平均摩尔质量
【答案】A
【解析】
试题由左图,温度相同时,p2>p1,压强越大,C%越大,所以x=1;压强相同时,T1>T2,温度越高,C%越小,正反应是放热反应。升高温度,A的转化率减小,压强越大,A的转化率越大,A正确;混合气体总质量守恒,容积固定,气体密度不变,B错误;升高温度,平衡向左移动,B的质量分数增大,C错误;升高温度,平衡向左移动,气体物质的量增大,气体总质量不变,平均摩尔质量减小,增大压强,气体摩尔质量增大,p3>p4,D错误。

 阅读快车系列答案
阅读快车系列答案【题目】电解法生产锰时会产生大量的阳极泥,其主要成分为MnO2和Pb,还含有少量其他金属化合物。下图是回收电解锰阳极泥生产MnCO3的工艺流程。
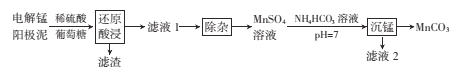
已知:Al(OH)3、Mn(OH)2、MnCO3的Ksp分别为1.0×10-33、1.9×10-13、2.2×10-11。
(l)“还原酸浸”时氧化产物为CO2,发生反应的化学方程式为____。
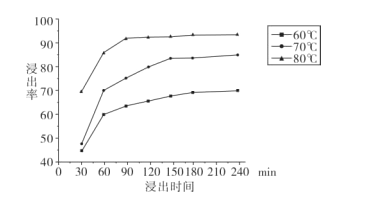
(2)“还原酸浸”实验中,锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为 ____ 。
(3)滤液l中的阳离子组成见下表:
组成 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
浓度/(mol·L-1) | 0.85 | 2.4×10-3 | 1.0×10-2 | 2.0×10-3 |
“除杂”时先加MnO2,MnO2的作用为 ___。
再加氨水调节pH使杂质离子沉淀完全,通过计算说明Al3+沉淀完全时Mn2+是否开始沉淀 ___。
(4)“沉锰”时发生反应的离子方程式为 ___。
(5)“沉锰”的关键操作有2点:①将NH4HCO3溶液滴入MnSO4溶液中;②反应终点pH=7。如果颠倒试剂滴加顺序,将MnSO4溶液滴人NH4HCO3,溶液中,或反应终点pH>7可能造成同样的后果,该后果是____;如粜反应终点pH<7,可能的后果是______。
(6)从滤液2中回收得到的副产品的用途为________。
【题目】Ⅰ.K2Cr2O7的水溶液中存在如下平衡:Cr2O72-(aq)+ H2O(l)![]() 2CrO42-(aq)+ 2H+(aq),平衡常数表达式为__;往上述溶液中加入氢氧化钠溶液现象为___;此实验现象,符合勒夏特列原理:如果改变维持化学平衡的条件(浓度、压力和温度),平衡就会向着__这种改变的方向移动。
2CrO42-(aq)+ 2H+(aq),平衡常数表达式为__;往上述溶液中加入氢氧化钠溶液现象为___;此实验现象,符合勒夏特列原理:如果改变维持化学平衡的条件(浓度、压力和温度),平衡就会向着__这种改变的方向移动。
Ⅱ. 为了证明化学反应有一定的限度,利用铁离子可以氧化碘离子的反应进行了如下探究活动:
(1)步骤1:取8mL0.1molL﹣1的KI溶液于试管,滴加0.1molL﹣1的FeCl3溶液5~6滴,振荡;
步骤2:在上述试管中加入2mLCCl4,充分振荡、静置;
步骤3:取上述步骤2静置分层后的上层水溶液少量于试管,滴加5~6滴0.1molL﹣1___(试剂名称),振荡,未见溶液呈血红色。
(2)探究的目的是通过检验Fe3+,来验证是否有Fe3+残留,从而证明化学反应有一定的限度。针对实验现象,同学们提出了下列两种猜想:
猜想一:________________
猜想二:Fe3+大部分转化为Fe2+,使生成Fe(SCN)3浓度极小,肉眼无法观察其颜色
为了验证猜想,在查阅资料后,获得下列信息:
信息一:Fe3+可与[Fe(CN)6]4﹣反应生成蓝色沉淀,反应的离子方程式为___,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高。
信息二:乙醚比水轻且微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大。
结合新信息,请你完成以下实验:各取少许步骤3的水溶液分别于试管A、B中,请将相关的实验操作、预期现象和结论填入下表空白处:
实验操作 | 预期现象 | 结论 |
实验1:①___________ | ②______ | 则“猜想一”不成立 |
实验2:在试管B加入少量乙醚,充分振荡,静置 | ③______ | 则“猜想二”成立 |
【题目】欲测定某NaOH溶液的物质的量浓度,可用0.100 0 mol·L-1的HCl标准溶液进行中和滴定(用甲基橙作指示剂)。请回答下列问题:
(1)滴定时,盛装待测NaOH溶液的仪器名称为________。
(2)滴定至终点的颜色变化为____________。
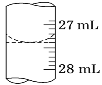
(3)若甲学生在实验过程中,记录滴定前滴定管内液面读数为0.50 mL,滴定后液面如图,则此时消耗标准溶液的体积为__________。
(4)乙学生做了三组平行实验,数据记录如下:
实验 序号 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 HCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 26.29 |
2 | 25.00 | 1.00 | 31.00 |
3 | 25.00 | 1.00 | 27.31 |
选取上述合理数据,计算出待测NaOH溶液的物质的量浓度为______。(保留四位有效数字)
(5)下列哪些操作会使测定结果偏高________(填字母)。
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后再用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数