题目内容
研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2。他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)( )
| A.0.448L | B.2.240L | C.2.016L | D.无法确定 |
C
解析试题分析:根据氧化还原反应的得失电子守恒规律,KMnO4中Mn得到的电子总数,等于KMnO4中O失去的电子总数与浓盐酸中氯离子失去电子变为氯气失去的电子总数之和.6.32gKMnO4的物质的量n=n/M═6.32g/158g/mol=0.04mol,0.112LO2的物质的量="V/Vm=0.112L/22.4L/" mol=0.005mol
得到的电子:KMnO4~5e-~Mn2+,K2MnO4~4e-~Mn2+,MnO2~2e-~Mn2+,
失去的电子:2Cl-~2e-~Cl2
根据电子守恒计算:
n(KMnO4)×5e-=n(O2)×4e-+n(Cl2)×2e-
0.04mol×5e-=0.005mol×4e-+n(Cl2)×2e-
n(Cl2)=0.09mol
所以生成的氯气标准状况下的体积V(Cl2)=n×Vm=0.09mol×22.4L/mol=2.016L.故选C.
考点:氧化还原反应的电子守恒的计算应用

 阅读快车系列答案
阅读快车系列答案高铁酸钠(Na2FeO4)是一种新型、高效、多功能的水处理剂。湿法制备的离子反应方程式: 2Fe(OH)3+3ClO-+4OH-→ 2FeO42-+3Cl-+5H2O;干法制备化学反应方程式:2FeSO4+4Na2O2→2Na2FeO4+2Na2SO4。有关分析错误的是
| A.等物质的量Na2FeO4氧化能力优于次氯酸钠 |
| B.湿法中氢氧化铁被氧化 |
| C.干法中每生成1 mol Na2FeO4转移3 mol电子 |
| D.高铁酸钠的氧化性大于次氯酸钠 |
根据表中信息判断,下列选项不正确的是
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-… | Cl2、Mn2+… |
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑,对于该反应,下列判断正确的是
| A.NaN3中氮元素的化合价为—3 |
| B.氧化剂和还原剂是同一物质 |
| C.反应过程中若转移1mol电子,则产生2.24L气体(标准状况) |
| D.被氧化的氮原子与生成的氮气分子个数之比为15:8 |
三氟化氮(NF3)(提示氟只有两种价态:-1,0)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2molHNO3,则转移0.2mol电子 |
| D.若1molNF3被氧化反应转移电子数为2NA |
下列变化需要加入适当的氧化剂才能实现的是
A.CuO Cu Cu | B.Fe2+ Fe Fe | C.H2SO4 SO2 SO2 | D.HCl Cl2 Cl2 |
某溶液中含有大量的Cl一、Br一、I一,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br一、I一的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl一、Br一、I一的物质的量浓度之比为( )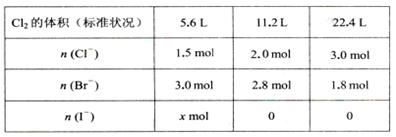
| A.5:15:4 | B.5:12:4 | C.15 : 30 : 8 | D.条件不足,无法计算 |
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。工业上可通过以下反应制得ClO2:2NaClO3+Na2SO3+H2SO4= 2ClO2↑+2Na2SO4 + H2O。下列说法正确的是
| A.氯元素的化合价升高 | B.Na2SO3是还原剂 |
| C.NaClO3发生氧化反应 | D.H2SO4被还原 |
向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
| A.Cu与Cu2O 的物质的量之比为2:1 |
| B.硝酸的物质的量浓度为2.6mol/L |
| C.产生的NO在标准状况下的体积为4.48L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol |