题目内容
在温度相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒压,发生反应CH3OCH3(g)+H2O(g) 2CH3OH(g);△H=37kJ·mol-1,测得反应达到平衡时的有关数据如下:
2CH3OH(g);△H=37kJ·mol-1,测得反应达到平衡时的有关数据如下:
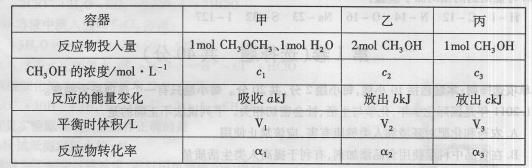
下列说法正确的是 ( )
 2CH3OH(g);△H=37kJ·mol-1,测得反应达到平衡时的有关数据如下:
2CH3OH(g);△H=37kJ·mol-1,测得反应达到平衡时的有关数据如下:
下列说法正确的是 ( )
A.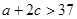 | B.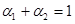 | C.V1=2V3 | D.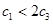 |
BCD
恒温、恒压条件下,对于等体积的可逆反应来说,如果投料量转化成相同物质时,量成比例,则建立的平衡是等效的;甲、乙、丙三种投料方式采用“一边倒”的形式转化成CH3OH时,量成比例,达到平衡时均互为等效平衡,达到平衡后,各组分的百分含量相同;等效平衡可分为全等效、半等效;甲与乙投料量转化成CH3OH时量相同,达平衡时为全等级效(各组分的百分含量、浓度、物质的量均相同),乙与丙投料量不同相差一半,属于半等效,平衡时各组分的百分含量、各组分的浓度相同,但各组分的物质的量相关一半。
CH3OCH3(g)+H2O(g) 2CH3OH(g);△H=37kJ·mol-1,
2CH3OH(g);△H=37kJ·mol-1,
1mol 1mol 0 37
x x 2x a=37x
1-x 1-x 2x
2CH3OH(g) CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
2mol 0 0 -37
2y y y b= 18.5y
2-2y y y
2CH3OH(g) CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
1mol 0 0 -37
2z z z c= 18.5z
1-2z z z
因甲、丙互为半等效,所以得:1-x=z; a="37x" ;c=18.5z=18.5×(1-x)
2c="37-37x" ; a+2c=37x+37-37x=37;A错;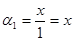 ;
;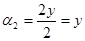 ;又因甲与乙互为全等效,所以得1-x=y;即
;又因甲与乙互为全等效,所以得1-x=y;即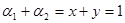 ,B正确;由于该反应为等体积反应,反应前后气体总物质的量不变,所以平衡时
,B正确;由于该反应为等体积反应,反应前后气体总物质的量不变,所以平衡时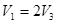 ,C正确; D错,平衡时
,C正确; D错,平衡时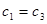 答案错误。
答案错误。
CH3OCH3(g)+H2O(g)
 2CH3OH(g);△H=37kJ·mol-1,
2CH3OH(g);△H=37kJ·mol-1,1mol 1mol 0 37
x x 2x a=37x
1-x 1-x 2x
2CH3OH(g)
 CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,2mol 0 0 -37
2y y y b= 18.5y
2-2y y y
2CH3OH(g)
 CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,
CH3OCH3(g)+H2O(g)△H=-37kJ·mol-1,1mol 0 0 -37
2z z z c= 18.5z
1-2z z z
因甲、丙互为半等效,所以得:1-x=z; a="37x" ;c=18.5z=18.5×(1-x)
2c="37-37x" ; a+2c=37x+37-37x=37;A错;
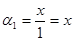 ;
;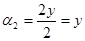 ;又因甲与乙互为全等效,所以得1-x=y;即
;又因甲与乙互为全等效,所以得1-x=y;即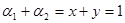 ,B正确;由于该反应为等体积反应,反应前后气体总物质的量不变,所以平衡时
,B正确;由于该反应为等体积反应,反应前后气体总物质的量不变,所以平衡时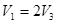 ,C正确; D错,平衡时
,C正确; D错,平衡时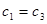 答案错误。
答案错误。
练习册系列答案
相关题目
 4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是
4C(g)+D(g);△H<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如下图。下列说法正确的是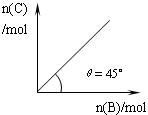
 醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应:
醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,在500oC下发生反应: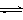 CH3OH(g)+H2O(g);△H=-49.0kJ/mol
CH3OH(g)+H2O(g);△H=-49.0kJ/mol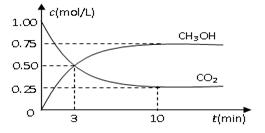
 _____;
_____; 为__________;
为__________; _____________________。
_____________________。 2E(g),若开始时只充入2 mol E(g),达平衡时,E的转化率为40%;若开始时充入2 mol M和1 mol N的混合气体,达平衡时混合气体的压强比起始时减少了
2E(g),若开始时只充入2 mol E(g),达平衡时,E的转化率为40%;若开始时充入2 mol M和1 mol N的混合气体,达平衡时混合气体的压强比起始时减少了 Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )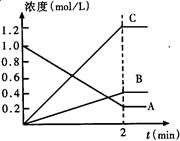
 3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。
3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表: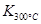 >
>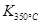 ,则该反应是 热反应。
,则该反应是 热反应。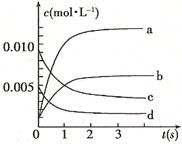
 状态的是
状态的是  。
。