��Ŀ����
��8�֣���2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g)  2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K= ����֪��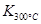 ��
��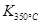 ����÷�Ӧ�� �ȷ�Ӧ��
����÷�Ӧ�� �ȷ�Ӧ��
��2����ͼ�б�ʾNO2�ı仯�������� ����O2��ʾ��0~2 s�ڸ÷�Ӧ��ƽ������v= ��
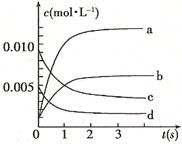
��3����˵���÷�Ӧ�Ѵﵽƽ�� ״̬����
״̬����  ��
��
a�� v(NO2)=2v(O2) b��������ѹǿ���ֲ���
c��v�� (NO)=2v��(O2) d���������ܶȱ��ֲ���
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ��� ��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����
 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
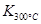 ��
��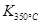 ����÷�Ӧ�� �ȷ�Ӧ��
����÷�Ӧ�� �ȷ�Ӧ����2����ͼ�б�ʾNO2�ı仯�������� ����O2��ʾ��0~2 s�ڸ÷�Ӧ��ƽ������v= ��

��3����˵���÷�Ӧ�Ѵﵽƽ��
 ״̬����
״̬����  ��
��a�� v(NO2)=2v(O2) b��������ѹǿ���ֲ���
c��v�� (NO)=2v��(O2) d���������ܶȱ��ֲ���
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ��� ��
a����ʱ�����NO2���� b���ʵ������¶�
c������O2��Ũ�� d��ѡ���Ч����

��

��ϰ��ϵ�д�
 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
�����Ŀ


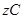 �ﵽƽ�⣺
�ﵽƽ�⣺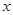 ��y��z��Ĺ�ϵ��________________��
��y��z��Ĺ�ϵ��________________��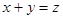 ��������ѹǿʱ����ƽ�ⷢ���ƶ�����һ����________����������桱����Ӧ�����ƶ���
��������ѹǿʱ����ƽ�ⷢ���ƶ�����һ����________����������桱����Ӧ�����ƶ��� 2CH3OH��g������H=37kJ��mol-1����÷�Ӧ�ﵽƽ��ʱ���й��������£�
2CH3OH��g������H=37kJ��mol-1����÷�Ӧ�ﵽƽ��ʱ���й��������£�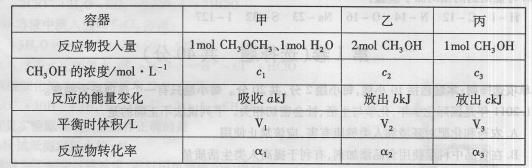
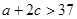
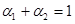
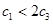
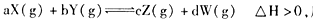 ��Ӧ5min�ﵽƽ��ʱ��X��Сn mol��L-1����Y��ʾ�ķ�Ӧ����Ϊ0.6n mol��L-1��min-1��������ϵѹǿ����W�İٷֺ����������仯��������������ȷ���� �� ��
��Ӧ5min�ﵽƽ��ʱ��X��Сn mol��L-1����Y��ʾ�ķ�Ӧ����Ϊ0.6n mol��L-1��min-1��������ϵѹǿ����W�İٷֺ����������仯��������������ȷ���� �� ��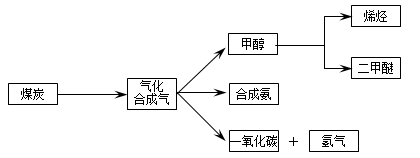
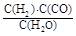 ��������Ӧ��Ӧ�Ļ�ѧ����ʽΪ ��
��������Ӧ��Ӧ�Ļ�ѧ����ʽΪ �� �¶�230��280�棩�������з�Ӧ��
�¶�230��280�棩�������з�Ӧ�� CH3OH(g) ��H1����90.7kJ��mol-1
CH3OH(g) ��H1����90.7kJ��mol-1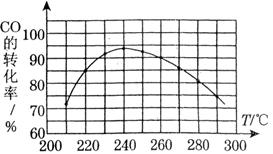
 ��
��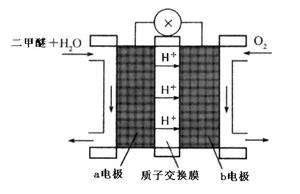
 2NH3 ��H��0����ʹ�ϳɰ���Ӧ���г̶�����ķ�����
2NH3 ��H��0����ʹ�ϳɰ���Ӧ���г̶�����ķ����� ���¶ȷֱ�ΪT1��T2ʱ,X��ת����
���¶ȷֱ�ΪT1��T2ʱ,X��ת����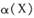 ��ʱ��仯�Ĺ�ϵ����ͼ��ʾ�������н�����ȷ����
��ʱ��仯�Ĺ�ϵ����ͼ��ʾ�������н�����ȷ����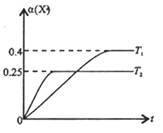
 ����С��Y��ת����
����С��Y��ת����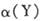 Ҳ��С
Ҳ��С
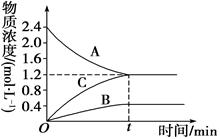
 �ݰ�������ѧƽ�⡢����ƽ�⡢ˮ��ƽ���
�ݰ�������ѧƽ�⡢����ƽ�⡢ˮ��ƽ��� 4C(g) ��H>0�ﵽƽ��ʱ��c(A)=2mol��L��c(B)=7mol��L��c(c)
4C(g) ��H>0�ﵽƽ��ʱ��c(A)=2mol��L��c(B)=7mol��L��c(c)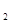 (g)
(g) 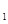 ��K
��K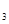 ��ƽ�ⳣ��K=19���ڸ��¶��µ����
��ƽ�ⳣ��K=19���ڸ��¶��µ����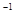 c0(O
c0(O
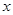 kJ��mol
kJ��mol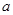 +b>
+b>