题目内容
在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。已知:K(300℃)>K(350 ℃),则该反应正反应是 热反应。
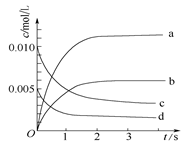
(2)图中表示NO2的变化的曲线是 。用O2表示从0~2 s内该反应的平均速率v(O2)= 。
(3)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(1)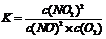 放 (2)b 1.5×10-3 mol/(L·s) (3)bc (4)c
放 (2)b 1.5×10-3 mol/(L·s) (3)bc (4)c
解析试题分析:试题分析:(1)化学平衡常数是可逆反应达到平衡状态时,各生成物浓度幂指数的乘积与个反应物浓度幂指数乘积的比。对于该反应来说,化学平衡常数为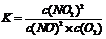 。由于K(300℃)>K(350 ℃),说明升高温度,化学平衡逆向移动。根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,逆反应为吸热反应,所以正反应为放热反应。(2)反应开始时,c(NO)= 0.020mol÷2L=0.01mol/L,当反应达到平衡时,c(NO)= 0.007mol÷2L=0.0035mol/L.而NO2开始时浓度为0,达到平衡时,由方程式2NO(g)+O2(g)
。由于K(300℃)>K(350 ℃),说明升高温度,化学平衡逆向移动。根据平衡移动原理,升高温度,化学平衡向吸热反应方向移动,逆反应为吸热反应,所以正反应为放热反应。(2)反应开始时,c(NO)= 0.020mol÷2L=0.01mol/L,当反应达到平衡时,c(NO)= 0.007mol÷2L=0.0035mol/L.而NO2开始时浓度为0,达到平衡时,由方程式2NO(g)+O2(g) 2NO2(g)中NO与NO2的关系可知b是NO2的变化的曲线。V(NO)= (0.01mol/L-0.004mol/L)÷2s=0.003mol/(L·s).V(O2):V(NO)=1:2,所以.V(O2)=1/2×V(NO)= 1/2× 0.003mol/(L·s)= 1.5×10-3 mol/(L·s).(3)A.在任何时刻都存在v(NO2)=2v(O2),所以不能作为判断平衡的标准。错误。B.由于该反应是反应前后气体体积不等的可逆反应,若反应未达到平衡,容器内的气体的物质的量就要腐蚀变化,容器内压强也要变化。若压强保持不变,则说明气体的物质的量都不变化。反应达到平衡状态。正确。C.在任何时刻的存在v正(NO)=2v正(O2);而v逆(NO)=2v正(O2)说明v正(NO)= v逆(NO)。所以反应达到平衡。正确。D.由于容器的容积不变,反应遵循质量守恒定律,所以无论反应进行到什么程度,容器内密度都始终保持不变。因此不能作为判断是否达到平衡的标准。错误。(4)A. 及时分离出NO2气体,即减小生成物的浓度,平衡正向移动,但是由于浓度减小,所以化学反应速率减慢。错误。B.适当升高温度,化学反应速率加快。但是由于该反应的正反应为放热反应。所以根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,即向逆反应方向移动。错误。C.增大O2的浓度。增大反应物的浓度,化学反应速率加快。根据平衡移动原理:增大反应物的浓度,化学平衡向正反应方向移动。正确。D.选择高效催化剂可以提高化学反应速率。但是化学平衡不发生移动。错误。
2NO2(g)中NO与NO2的关系可知b是NO2的变化的曲线。V(NO)= (0.01mol/L-0.004mol/L)÷2s=0.003mol/(L·s).V(O2):V(NO)=1:2,所以.V(O2)=1/2×V(NO)= 1/2× 0.003mol/(L·s)= 1.5×10-3 mol/(L·s).(3)A.在任何时刻都存在v(NO2)=2v(O2),所以不能作为判断平衡的标准。错误。B.由于该反应是反应前后气体体积不等的可逆反应,若反应未达到平衡,容器内的气体的物质的量就要腐蚀变化,容器内压强也要变化。若压强保持不变,则说明气体的物质的量都不变化。反应达到平衡状态。正确。C.在任何时刻的存在v正(NO)=2v正(O2);而v逆(NO)=2v正(O2)说明v正(NO)= v逆(NO)。所以反应达到平衡。正确。D.由于容器的容积不变,反应遵循质量守恒定律,所以无论反应进行到什么程度,容器内密度都始终保持不变。因此不能作为判断是否达到平衡的标准。错误。(4)A. 及时分离出NO2气体,即减小生成物的浓度,平衡正向移动,但是由于浓度减小,所以化学反应速率减慢。错误。B.适当升高温度,化学反应速率加快。但是由于该反应的正反应为放热反应。所以根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动,即向逆反应方向移动。错误。C.增大O2的浓度。增大反应物的浓度,化学反应速率加快。根据平衡移动原理:增大反应物的浓度,化学平衡向正反应方向移动。正确。D.选择高效催化剂可以提高化学反应速率。但是化学平衡不发生移动。错误。
考点:考查化学平衡常数的表达式、化学反应速率的计算及外界条件对化学反应速率和化学平衡移动的影响的知识。

在密闭容器中,一定条件下进行如下反应NO(g)+CO(g)
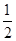 N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+CO2(g),ΔH=-373.2 kJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应4~8 min间的平均反应速率和推测反应16 min时反应物的浓度,结果应是( )
| A.2.5 μmol·L-1·min-1和2.0 μmol·L-1 |
| B.2.5 μmol·L-1·min-1和2.5 μmol·L-1 |
| C.3.0 μmol·L-1·min-1和3.0 μmol·L-1 |
| D.5.0 μmol·L-1·min-1和3.0 μmol·L-1 |
合成氨反应的正反应是气体体积减小的放热反应。合成氨工业的生产流程如下: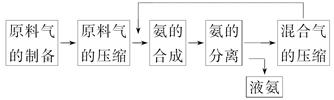
关于合成氨工业的说法中不正确的是( )
| A.混合气进行循环利用遵循绿色化学思想 |
| B.合成氨反应须在低温下进行 |
| C.对原料气进行压缩是为了增大原料气的转化率 |
| D.使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动 |
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+SCN-(aq)  Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
| A.FeCl3(aq)与KSCN(aq)反应的热化学方程式为:Fe3+(aq)+SCN-(aq)=Fe(SCN)2+(aq) ΔH>0 |
| B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2 |
| C.反应处于D点时,一定有v(正)>v(逆) |
| D.A点与B点相比,A点的c(Fe3+)大 |
关于可逆反应mA(g)+nB(g)  pC(g)+qD(g)及其图象的说法正确的是( )
pC(g)+qD(g)及其图象的说法正确的是( )
| A.若图象为Ⅰ,则m+n>p+q |
| B.若图象为Ⅱ,则m+n=p+q,t2时刻改变的条件一定是使用催化剂 |
| C.若图象为Ⅲ,则该可逆反应的ΔH<0 |
| D.若图象为Ⅳ,且压强p1>压强p2,则该可逆反应的ΔH>0 |
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g) ΔH="Q" kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g) ΔH="Q" kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
| 气体体积/L c(Y)/(mol·L-1) 温度/℃ | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
下列说法正确的是( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减小
D.体积不变,温度升高,平衡向逆反应方向移动
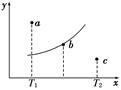
 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是( )
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有 a、b、c三点,如图所示,则下列描述正确的是( )