题目内容
下列有关物质的性质、应用或制取的说法正确的是( )
| A、工业上将氯气通入澄清石灰水中,制取漂白粉 |
| B、除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤 |
| C、自来水厂可用明矾对水进行消毒杀菌 |
| D、常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸 |
考点:氯气的化学性质,盐类水解的应用,硝酸的化学性质
专题:元素及其化合物,化学应用
分析:A.氯气与石灰乳制备漂白粉;
B.碳酸钙与盐酸反应生成氯化钙;
C.明矾不具有强氧化性;
D.常温下浓硝酸与铝发生钝化.
B.碳酸钙与盐酸反应生成氯化钙;
C.明矾不具有强氧化性;
D.常温下浓硝酸与铝发生钝化.
解答:
解:A.氯气与石灰乳制备漂白粉,而石灰水中含溶质较少,不能制备漂白粉,故A错误;
B.碳酸钙与盐酸反应生成氯化钙,且不引人新杂质,则反应后过滤可除杂,故B正确;
C.明矾不具有强氧化性,不能杀菌消毒,但水解生成胶体可除去水中悬浮杂质,故C错误;
D.常温下浓硝酸与铝发生钝化,为氧化还原反应,生成致命的氧化膜阻止反应的进一步发生,故D错误;
故选B.
B.碳酸钙与盐酸反应生成氯化钙,且不引人新杂质,则反应后过滤可除杂,故B正确;
C.明矾不具有强氧化性,不能杀菌消毒,但水解生成胶体可除去水中悬浮杂质,故C错误;
D.常温下浓硝酸与铝发生钝化,为氧化还原反应,生成致命的氧化膜阻止反应的进一步发生,故D错误;
故选B.
点评:本题考查物质的性质,综合考查元素化合物,为高频考点,把握物质的性质及发生的反应为解答的关键,注意性质与用途的关系,题目难度不大.

练习册系列答案
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
下列叙述正确的是( )
①久置于空气中的氢氧化钠溶液,加盐酸时有气体产生
②浓硫酸可用于干燥氨气、二氧化氮气体
③SiO2和CO2都是酸性氧化物,都能与强碱溶液反应,但不能与任何酸反应
④玻璃、水泥、水晶项链都是硅酸盐制品
⑤蔗糖炭化的演示实验中,浓硫酸既体现了其强氧化性又体现了其脱水性.
①久置于空气中的氢氧化钠溶液,加盐酸时有气体产生
②浓硫酸可用于干燥氨气、二氧化氮气体
③SiO2和CO2都是酸性氧化物,都能与强碱溶液反应,但不能与任何酸反应
④玻璃、水泥、水晶项链都是硅酸盐制品
⑤蔗糖炭化的演示实验中,浓硫酸既体现了其强氧化性又体现了其脱水性.
| A、①④⑤ | B、①⑤ |
| C、②③④ | D、④⑤ |
X、Y、Z、W四种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为17.其中W的阴离子核外电子数与Z原子的最内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Y、Z均能形成双原子分子.根据以上叙述,下列说法中正确的是( )
| A、以上四种元素的原子半径大小为X<Y<Z<W |
| B、X2W2、W2Y、WZ均为直线型的共价化合物 |
| C、W与Y形成的化合物W2Y2在化学反应中既可作氧化剂也可作还原剂 |
| D、由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
SO2是常见的大气污染物之一.我国规定空气中其含量不得超过0.02mg/L.下列措施,能够减少SO2排放量的是( )
①用天然气代替煤炭作民用燃料
②提高热能利用率
③硫酸厂采用更好的催化剂使SO2转化为SO3
④使用CS2萃取煤炭中的硫
⑤燃煤中加入生石灰后使用.
①用天然气代替煤炭作民用燃料
②提高热能利用率
③硫酸厂采用更好的催化剂使SO2转化为SO3
④使用CS2萃取煤炭中的硫
⑤燃煤中加入生石灰后使用.
| A、全部 | B、①②⑤ |
| C、①③⑤ | D、①③④ |
m g铜和足量的浓硫酸反应,生成SO2 n L,则被还原的硫酸是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列物质间的反应,其能量变化符合如图的是( )


| A、铁与硫粉在加热条件下的反应 |
| B、灼热的碳与二氧化碳反应 |
| C、Ba(OH)2?8H2O晶体和NH4Cl晶体混合 |
| D、碳酸钙的分解 |
下列微粒的核外电子的表示方法中正确的是( )
A、基态碳原子的电子排布图 |
B、基态铜原子核外的3d、4s轨道内电子排布图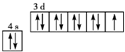 |
| C、Cl的外围电子排布式3s13p6 |
| D、Fe2+的电子排布式1s22s22p63s23p63d6 |
X、Y、Z三种元素,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
| A、N、P、O |
| B、N、C、Si |
| C、B、Mg、Al |
| D、C、N、P |
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶