题目内容
【题目】为探究外界条件对反应:mA(g)+nB(g)cZ(g) ΔH 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是 ( )
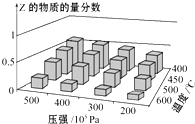
A.在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平衡时,Z的物质的量分数不变
B.升高温度,正、逆反应速率都增大,平衡常数增大
C.ΔH>0,m+n>c
D.温度不变,增大压强,平衡正向移动,达新平衡时,A的浓度比原平衡减小
【答案】A
【解析】
在恒温环境下,压强增大,Z的物质的量增大,平衡正向移动,根据勒夏特列原理可知,m+n>c;在恒压环境下,温度升高,Z的物质的量减小,平衡逆向移动,根据勒夏特列原理,反应放热,据此回答问题。
A.在恒温恒压条件下,向已达到平衡的体系中加入少量Z,为保持压强不变体积增大,由于生成物只有一种,故投料配比与原投料相同,达新平衡时与原平衡等效,Z的物质的量分数不变,A正确;
B.根据有效碰撞理论,升高温度,正、逆反应速率都增大,但是平衡逆向移动,平衡常数减小,B错误;
C.正反应是放热的,则△H<0,减小压强,化学平衡是向着气体系数和增加的方向进行的,所以有m+n>c, C错误;
D.根据图像可知,若保持温度不变时增大压强,因体积减小,各组分的浓度变大,虽然平衡正向移动,但是根据平衡移动原理可知,达新平衡时,A的浓度比原平衡增大,D错误。
答案为A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目