题目内容
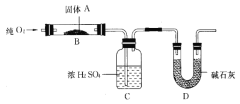
【题目】某同学用如下图所示装置(I)制取溴苯和溴乙烷。已:溴乙烷为无色液体,难溶于水,沸点38.4℃,熔点一119℃,密度为1.64g·cm-3。主要实验步骤如下:

①检查气密性后,向烧瓶中加入一定量苯和液溴。
②向锥型瓶中加入乙醇和浓H2SO4的混合液至恰好没过进气导管口。
③将A装置中纯铁丝小心向下插入混合液中。
④点燃B装置中酒精灯,用小火缓缓对锥形瓶加热10分钟。
请填写下列空白:
(1)A装置中发生的反应的化学方程式________________________________
(2)导管a的作用是_______________。
(3)C装置中U型管的内部用蒸馏水封住管底的作用是___________________________。
(4)反应完毕后,分离出溴乙烷时所用最主要仪器名称是(只填一种)_____________。
(5)步骤④中可否用大火加热,理由是____________________________________。
(6)为证明溴和苯的上述反应是取代而不是加成反应。该学生用装置(Ⅱ)代替装置B、C直接与A相连接重新反应,锥形瓶里盛放的液体为AgNO3溶液。
①装置(Ⅱ)的锥形瓶中小试管内的液体是____________(填名称),其作用为_______________
②能证明溴和苯的反应是取代反应的现象为_________________________;装置(Ⅱ)还可起到的作用是_______________。
【答案】![]() +Br2
+Br2 ![]()
![]() +HBr 导气、冷凝、回流 溶解吸收溴化氢气体,防止溴化氢及产物逸出污染环境 分液漏斗 不能,易发生副反应生成乙醚、乙烯等 CCl4 吸收挥发出来的溴蒸气 锥形瓶中生成淡黄色沉淀 防止倒吸
+HBr 导气、冷凝、回流 溶解吸收溴化氢气体,防止溴化氢及产物逸出污染环境 分液漏斗 不能,易发生副反应生成乙醚、乙烯等 CCl4 吸收挥发出来的溴蒸气 锥形瓶中生成淡黄色沉淀 防止倒吸
【解析】
(1)A装置中苯在铁做催化剂时可以和溴发生取代反应获得溴苯,发生反应的原理方程式为: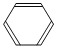 +Br2
+Br2 ![]()
![]() +HBr,故答案为:
+HBr,故答案为: +Br2
+Br2 ![]()
![]() +HBr;
+HBr;
(2)苯和溴都是易挥发的物质,导管a起导气,兼起苯与溴蒸气的冷凝和回流作用,减少反应物的损失,故答案为:导气、冷凝、回流;
(3)溴化氢极易溶于水,形成的氢溴酸是强酸,水可以阻止易挥发物质HBr的溢出,起到水封的作用,故答案为:溶解吸收溴化氢气体,防止溴化氢及产物逸出污染环境;
(4)反应完毕后,分离U形管内有溴乙烷和蒸馏水,溴乙烷不溶于水,所以分离出溴乙烷要用分液的方法,用到的主要仪器是分液漏斗,故答案为:分液漏斗;
(5)步骤④不能用大火加热,否则乙醇在浓H2SO4存在条件下发生副反应生成乙醚、乙烯等,故答案为:不能,易发生副反应生成乙醚、乙烯等;
(6)①苯和溴都是易挥发的物质,生成物中有苯和溴蒸气,要除去,所以装置(Ⅱ)的锥形瓶中,小试管内盛有CCl4液体,其作用是吸收挥发出来的溴蒸气,故答案为:CCl4;吸收挥发出来的溴蒸气;
②除去苯和溴蒸气的HBr被锥形瓶里盛放的液体为AgNO3溶液吸收,生成淡黄色的溴化银沉淀,说明溴和苯的反应是取代反应;HBr极易溶于水,装置(Ⅱ)还可起到防止倒吸的作用,故答案为:锥形瓶中生成淡黄色沉淀;防止倒吸。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】下列实验操作、现象及所得出的结论或解释均正确的是
选项 | 实验操作 | 现象 | 结论或解释 |
A | 向盐酸中滴加Na2SO3溶液 | 产生使品红溶液褪色的气体 | 非金属性:Cl>S |
B | 向废FeCl3蚀刻液X中加入少量的铁粉,振荡 | 未出现红色固体 | X中一定不含Cu2+ |
C | 用c(Fe3+)相同的Fe2(SO4)3和FeCl3溶液,分别清洗做完银镜反应的试管 | FeCl3溶液清洗得较干净 | Fe3++Ag |
D | 用3 mL稀硫酸与纯锌粒反应,再加入几滴 Cu(NO3)2浓溶液 | 迅速产生无色气体 | 形成Zn-Cu原电池加快了制取H2的速率 |
A. A B. B C. C D. D