题目内容
【题目】既含离子键又含共价键的物质是
A. H2 B. NaOH C. H2O D. MgC12
【答案】B
【解析】
一般来说,活泼金属元素与活泼非金属元素形成离子键,非金属元素之间形成共价键,
A项、H2是双原子分子,分子中只有共价键,故A错误;
B项、NaOH是由钠离子和氢氧根离子构成的离子化合物,钠离子和氢氧根之间是离子键,氢氧根内部存在共价键,故B正确;
C项、H2O是共价化合物,分子中只有共价键,故C错误;
D项、MgC12是离子化合物,只存在镁离子和氯离子之间的离子键,故D错误。
故选B。

【题目】碳酸镁晶须是一种新型吸波隐形材料中的增强剂。某工厂以MgCl2(含少量杂质FeCl2、FeCl3)为原料制备碳酸镁晶须(MgCO3·H2O)的工艺流程如下:
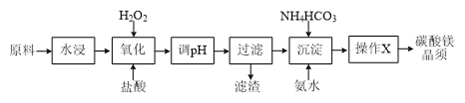
已知:Fe3+、Fe2+、Mg2+生成氢氧化物沉淀时的pH
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.6 |
Mg(OH)2 | 9.9 | 11.1 |
注:Fe(OH)2沉淀呈絮状,不易从溶液中除去。
(1)写出“氧化”过程中发生的离子反应方程式并用双线桥标出电子转移的方向和数目____。
(2)pH调节的范围______,滤渣的主要成分______(填化学式)。
(3)操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法_____。
(4)水浸后溶液中Fe2+、Fe3+含量的测定
①取水浸后溶液100.00 mL,测得Cl的浓度为0.455 mol·L1,向其中缓缓通入氯气使Fe2+恰好完全转化为Fe3+,测得此时溶液中Cl的浓度为0.460 mol·L1(溶液体积变化忽略不计)。
②另取水浸后溶液100.00 mL,向其中加入过量的1 mol·L1 NaOH溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为0.96 g。
试通过计算确定水浸后溶液中Fe2+、Fe3+的物质的量浓度______(写出计算过程)。