题目内容
【题目】海洋中有丰富的资源,下图为海水利用的部分过程。下列有关说法正确的是
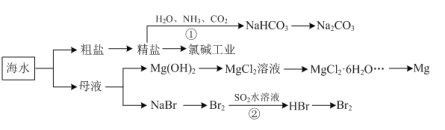
A.由反应①可知:相同温度下,NaHCO3的溶解度大于Na2CO3
B.MgCl2溶液通过蒸发浓缩、冷却结晶可获得MgCl2·6H2O
C.反应②的离子方程式为:Br2+SO2+2H2O=SO42—+2Br—+4H+
D.粗盐中含有的Mg2+、SO42—等杂质离子,可通过依次加入BaCl2溶液、NaOH溶液、盐酸等试剂加以去除
【答案】BC
【解析】
A. 相同温度下,NaHCO3的溶解度小于Na2CO3,所以反应①能够发生,故A错误;
B. 氯化镁溶液通过蒸发浓缩,冷却结晶,过滤、洗涤、干燥可以得到六水氯化镁晶体,故B正确;
C. 反应②为溴与二氧化硫水溶液发生氧化还原反应生成硫酸和氢溴酸,反应的离子方程式为Br2+SO2+2H2O=SO42—+2Br—+4H+,故C正确;
D.依次加入氯化钡溶液、氢氧化钠溶液、盐酸等试剂无法除去溶液中过量的氯化钡,除去粗盐中含有的Mg2+、SO42—等杂质离子应该依次加入氯化钡溶液、氢氧化钠溶液、碳酸钠溶液、盐酸,故D错误;
故选BC。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案
相关题目