题目内容
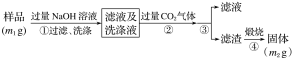
【题目】工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下(金属单质E可由滤液C制取):
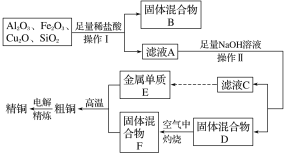
已知:Cu2O+2H+===Cu+Cu2++H2O。
(1)实验操作Ⅰ的名称为________;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有________(填仪器名称)。
(2)滤液A中铁元素的可能存在形式为________(填离子符号),生成该离子的方程式为_____,
若滤液A中存在Fe3+,检验该离子的试剂为________(填试剂名称)。
(3)金属E和固体F反应发生的某一反应可用于焊接钢轨,该反应化学方程式为_________。
【答案】过滤坩埚Fe2+(或Fe2+、Fe3+)Fe2O3+6H+===2Fe3++3H2O、2Fe3++Cu===2Fe2++Cu2+硫氰化钾溶液2Al+Fe2O3![]() Al2O3+2Fe
Al2O3+2Fe
【解析】
由流程图可以看出,SiO2与盐酸不反应,Fe2O3、Al2O3、Cu2O发生反应,Cu2O+2H+===Cu+Cu2++H2O、Fe2O3+6H+===2Fe3++3H2O、Al2O3+6H+===2Al3++3H2O,而2Fe3++Cu===2Fe2++Cu2+,可分析出滤液A中的离子一定有H+、Cu2+、Al3+、Fe2+,可能有Fe3+(Cu2O较少时),加入足量NaOH溶液后得到的固体混合物D为Fe(OH)3和Cu(OH)2,在空气中灼烧后得到的固体混合物F为Fe2O3和CuO,滤液C中含AlO2-,则金属单质E为Al,以此解答。
由流程图可以看出,SiO2与盐酸不反应,Fe2O3、Al2O3、Cu2O发生反应,Cu2O+2H+===Cu+Cu2++H2O、Fe2O3+6H+===2Fe3++3H2O、Al2O3+6H+===2Al3++3H2O,而2Fe3++Cu===2Fe2++Cu2+,可分析出滤液A中的离子一定有H+、Cu2+、Al3+、Fe2+,可能有Fe3+(Cu2O较少时),加入足量NaOH溶液后得到的固体混合物D为Fe(OH)3和Cu(OH)2,在空气中灼烧后得到的固体混合物F为Fe2O3和CuO,滤液C中含AlO2-,则金属单质E为Al,利用铝热反应可焊接钢轨。
(1)实验操作Ⅰ分离固体和液体混合物,为过滤操作;在空气中灼烧固体混合物Fe(OH)3和Cu(OH)2时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有坩埚;
(2)滤液A中铁元素的可能存在形式为Fe2+,生成该离子的方程式为Fe2O3+6H+===2Fe3++3H2O、2Fe3++Cu===2Fe2++Cu2+;
若滤液A中存在Fe3+,检验该离子的试剂为硫氰化钾溶液;
(3)金属Al和Fe2O3反应可用于焊接钢轨,该反应化学方程式为2Al+Fe2O3![]() Al2O3+2Fe。
Al2O3+2Fe。

 阅读快车系列答案
阅读快车系列答案