题目内容
8.若NA表示阿伏加德罗常数的数值,下列说法错误的是( )| A. | 1 mol H2O所含质子数为10NA | |
| B. | 在标准状况下,0.5NA个氯气分子所占的体积约是11.2L | |
| C. | 标准状况下,22.4 L汽油所含的分子数为NA | |
| D. | 1克氢气所含原子数约为6.02×1023 |
分析 A、水中含10个质子;
B、根据体积V=$\frac{N}{{N}_{A}}Vm$来计算;
C、标况下,汽油为液态;
D、氢气由氢原子构成.
解答 解:A、水中含10个质子,故1mol水中含10mol质子即10NA个,故A正确;
B、标况下,氯气的体积V=$\frac{N}{{N}_{A}}Vm$=$\frac{0.5{N}_{A}}{{N}_{A}/mol}×22.4L/mol$=11.2L,故B正确;
C、标况下,汽油为液态,不能根据气体摩尔体积来计算其物质的量和分子个数,故C错误;
D、氢气由氢原子构成,故1g氢气中含有的氢原子的物质的量n=$\frac{1g}{1g/mol}$=1mol,即含有6.02×1023个,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
19.下列实验装置或操作正确的是( )
| A. | 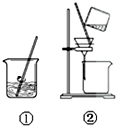 除去附着在铁屑表面的铝 | B. | 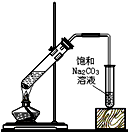 实验室制取乙酸乙酯 | ||
| C. | 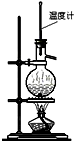 实验室制乙烯 | D. |  分离酒精和水 |
16.常温下,下列溶液中与1×10-5mol/L的NaOH溶液pH相同的是( )
| A. | 把pH=6的盐酸稀释1000倍 | |
| B. | 把pH=8的NaOH溶液稀释10倍 | |
| C. | 把10mL 1×10-5mol/L的H2SO4溶液与10mL 4×10-5mol/L的NaOH溶液相混合 | |
| D. | 把c(OH-)=10-5mol/L的NaOH溶液10mL加到100mL浓度为10-4mol/L的NaOH溶液中 |
3.下列说法正确的是( )
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应在一定条件下也能发生 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-235.8 kJ/mol 则氢气的燃烧热为235.8KJ/mol |
13.化学知识广泛应用于生产生活中,下列叙述正确的是( )
| A. | 空气中的臭氧对人体健康有益无害 | |
| B. | 液氯罐泄漏时,可将其移入水塘中并加入生石灰 | |
| C. | 工业用食盐水制取氯气过程中,不涉及氧化还原反应 | |
| D. | 日常生活中物体能够热胀冷缩是因为构成物质的微粒能够热胀冷缩 |
17.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 4.6 g C7H8和C3H8O3的混合物中所含氢原子总数为0.4NA | |
| B. | 标准状况下,11.2 L C2H5OH中所含的分子数为0.5NA | |
| C. | 常温常压下,0.1 mol Na2O2与CO2反应转移的电子数目为0.4NA | |
| D. | 在1 L 0.1 mol•L-1碳酸钠溶液中,阴离子总数等于0.1NA |
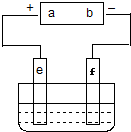 根据如图装置,按要求回答问题.
根据如图装置,按要求回答问题.