题目内容
3.下列说法正确的是( )| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 吸热反应在一定条件下也能发生 | |
| D. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-235.8 kJ/mol 则氢气的燃烧热为235.8KJ/mol |
分析 A、吸热反应不一定需要加热;
B、放热反应有些需要加热才能发生;
C、吸热反应也能发生;
D、燃烧热是指在101kP时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,H元素要生成液态水.
解答 解:A、吸热反应不一定需要加热,需要加热才能发生的不一定是吸热反应,即反应吸放热与反应条件无必然关系,故A错误;
B、放热反应有些需要加热才能发生,如煤炭的燃烧,故B错误;
C、只要条件合适,吸热反应也能发生,故C正确;
D、燃烧热是指在101kP时,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量,H元素要生成液态水,而此反应中生成的是水蒸汽,故不是氢气的燃烧热,故D错误.
故选C.
点评 本题考查了吸放热反应与反应条件的关系,应注意的是吸热反应不一定需要加热,需要加热才能发生的不一定是吸热反应,即反应吸放热与反应条件无必然关系.

练习册系列答案
相关题目
13.根据热化学方程S (s)+O2(g)═SO2 (g)△H=-297.23kJ/mol (反应在298K,101kPa下发生)分析下列说法正确的是( )
| A. | 标况下,燃烧1mol S吸收的热量为297.23 kJ | |
| B. | S (g)+O2 (g)═SO2 (g) 放出的热量大于297.23 kJ | |
| C. | S (g)+O2 (g)═SO2 (g)放出的热量小于297.23 kJ | |
| D. | 形成1 mol SO2 的化学键所释放的总能量大于断裂 1 molS (s)和 1mol O2 (g)的化学键所吸收的总能量 |
14.下列关于原电池说法正确的是( )
| A. | 由Al、Mg、稀硫酸溶液组成的原电池,其负极反应式为:Al-3e-═Al3+ | |
| B. | 由Al、Mg、NaOH溶液组成的原电池,其负极反应式为:Al-3e-+3OH-═Al(OH)3↓ | |
| C. | 由Fe、Zn、NaCl溶液组成的原电池,其负极反应式为:Fe-2e-═Fe2+ | |
| D. | 由Al、Cu、浓硝酸溶液组成的原电池,其负极反应式为:Cu-2e-═Cu2+ |
18.警察常从案发现场的人体气味来获取有用线索,人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9一十一烷酸内酯;⑤十八烷⑥已醛;⑦庚醛.下列说法正确的是( )
| A. | ①、②、⑥分子中碳原子数小于10,③、④、⑤分子中碳原子数大于10 | |
| B. | ①、②是无机物,③、⑤、⑦是有机物 | |
| C. | ①、②、③是酸性化合物,⑤不是酸性化合物 | |
| D. | ②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
8.若NA表示阿伏加德罗常数的数值,下列说法错误的是( )
| A. | 1 mol H2O所含质子数为10NA | |
| B. | 在标准状况下,0.5NA个氯气分子所占的体积约是11.2L | |
| C. | 标准状况下,22.4 L汽油所含的分子数为NA | |
| D. | 1克氢气所含原子数约为6.02×1023 |
15.据最新科技报告,科学家发现了新的氢微粒,它由3个氢原子核(质子)和2个电子构成,关于这种微粒的下列说法中正确的是( )
| A. | 一个该微粒含3个中子 | B. | 它是氢的一种新的同位素 | ||
| C. | 其组成可用H3+表示 | D. | 它比一个普通氢分子多一个氢原子 |
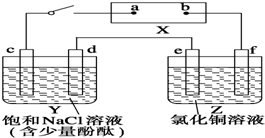 下图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.
下图中X是直流电源.Y槽中c、d为石墨棒,Z槽中e、f是质量相同的铜棒.接通电路后,发现d附近显红色.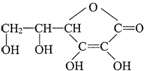 维生素C的结构简式是,它的分子式是C6H8O6;由于它能防治坏血病,又称为抗坏血酸.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐.离子方程式为Fe+2H+═Fe2++H2↑.
维生素C的结构简式是,它的分子式是C6H8O6;由于它能防治坏血病,又称为抗坏血酸.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性.市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分时盐酸)的作用下转化成亚铁盐.离子方程式为Fe+2H+═Fe2++H2↑.