题目内容
17.在某地农村曾发生过这样的事件:氮肥NH4NO3在运输过程中因淋雨而板结,为便于使用,人门试图将其敲砸粉碎. 意想不到的是NH4NO3受撞击迅速分解发生爆炸,造成人员伤亡.请你根据已有的化学知识,对安全使用已结块的NH4NO3提出合理的建议.
分析 依据题意硝酸铵因淋雨而板结,受撞击迅速分解发生爆炸,结合硝酸铵易溶于水的性质分析解答.
解答 解:依据题意硝酸铵因淋雨而板结,受撞击迅速分解发生爆炸,为了安全起见不能敲击板结的硝酸铵固体,硝酸铵极易溶于水,可以将其溶于水进行使用;
故答案为:为防止板结的硝酸铵固体敲击时产生爆炸,不能敲击板结的硝酸铵固体,硝酸铵极易溶于水,可以将其溶于水进行使用;
点评 本题考查了硝酸铵的性质,熟悉硝酸铵的性质是解题关键,题目难度不大.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
7.下列属于酸性氧化物的是( )
| A. | CO2 | B. | CaO | C. | K2SO4 | D. | NaOH |
8. 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
①已知:2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1;2H2(g)+O2(g)═2H2O(g)△H3=-484kJ•mol-1.则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-651kJ•mol-1;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:
A)在上述三种温度中,曲线Z对应的温度是270℃.
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K=4L2•mol-2.(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
若5min~10min只改变了某一条件,所改变的条件是增大H2的浓度;且该条件所改变的量是增大了0.1mol•L-1.
 甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1
甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产.工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)?CH3OH(g)△H1=-116kJ•mol-1①已知:2CO(g)+O2(g)═2CO2(g)△H2=-566kJ•mol-1;2H2(g)+O2(g)═2H2O(g)△H3=-484kJ•mol-1.则表示1mol气态甲醇完全燃烧生成CO2和水蒸气时的热化学方程式为CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g)△H=-651kJ•mol-1;
②在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律.如图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系.请回答:
A)在上述三种温度中,曲线Z对应的温度是270℃.
B)利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)?CH3OH(g)的平衡常数K=4L2•mol-2.(写明单位)
③在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
5.下列除杂方法不合理的是( )
| A. | 通过饱和食盐水除去Cl2中的HCl | |
| B. | 通过NaOH溶液除去CO2中的HCl | |
| C. | 通过加热法除去Na2CO3固体中的NaHCO3 | |
| D. | 通过NaOH溶液除去CO中混有的CO2 |
12.下列各组物质中,互为同系物的是( )
| A. | O2、O3 | B. |  | ||
| C. | 2-甲基丙烷、乙烷 | D. | 油酸、硬脂酸 |
2.配制500mL 0.1mol/L的硫酸铜溶液,需用胆矾(CuSO4•5H2O)( )
| A. | 8.00g | B. | 16.0g | C. | 25.0g | D. | 12.5g |
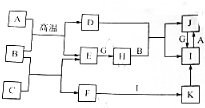 有关物质的转化关系如图所示(部分物质和条件已略去).A、C、E、G是中学化学中的常见单质,其中G呈黄绿色.E在G中燃烧发生苍白色火焰,F的焰色反应显黄色,B是常见的无色液体,K为红褐色沉淀.请回答下列问题:
有关物质的转化关系如图所示(部分物质和条件已略去).A、C、E、G是中学化学中的常见单质,其中G呈黄绿色.E在G中燃烧发生苍白色火焰,F的焰色反应显黄色,B是常见的无色液体,K为红褐色沉淀.请回答下列问题: .
.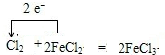 .
. )、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).
)、乙醛(CH3CHO)、乙酸(CH3COOH)、乙醇(CH3CH2OH).