题目内容
化学反应原理在工业生产中具有十分重要的意义。
(1)工业生产可以用NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为 。
(2)已知反应Fe(s) +CO2(g)  FeO(s) +CO(g) ΔH ="a" kJ/mol
FeO(s) +CO(g) ΔH ="a" kJ/mol
测得在不同温度下,该反应的平衡常数K随温度的变化如下:
①该反应的化学平衡常数表达式K= ,a 0(填“>”、“<”或“=”)。在500℃ 2L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5 min后达到平衡时CO2的转化率为 ,生成CO的平均速率v(CO)为 。
②700℃反应达到平衡后,要使该平衡向右移动,其他条件不变时,可以采取的措施有
(填字母)。
| A.缩小反应器容积 | B.增加Fe的物质的量 |
| C.升高温度到900℃ | D.使用合适的催化剂 |
(1)2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;(2)c(CO)/c(CO2);>;50%;0.2mol/(Lmin);C。
解析试题分析:(1)第一步:2NH3(g)+CO2(g)?H2NCOONH4(l,氨基甲酸铵)△H1=-272KJ/mol,第二步:H2NCOONH4(l)?H2O(l)+H2NCONH2(s)△H2=138KJ/mol,根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)?H2O(l)+H2NCONH2(s)△H=-134kJ?mol-1;(2)①反应Fe(s)+CO2(g)═FeO(s)+CO(g)的平衡常数k=c(CO)/c(CO2)
,由表中数据可知,对于反应①,温度越高平衡常数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应进行,故a>0,
令平衡时参加反应的二氧化碳的物质的量为xmol,则:
Fe(s)+CO2(g)═FeO(s)+CO(g)
开始(mol):4 0
变化(mol):x x
平衡(mol):4-x x
所以x/4?x=1解得x=2,故二氧化碳的转化率为2/4×100%=50%,故CO表示的平均速率v(CO)=2mol
/2L×5min=0.2mol/(L?min)。②A、缩小反应器容积,压强增大,化学平衡不移动,故A错误;B.增加Fe的物质的量,不会引起化学平衡的移动,故B错误;C.升高温度到900℃,化学平衡正向移动,故C正确;D.使用合适的催化剂,不会引起化学平衡的移动,故D错误。
考点:化学平衡

 快乐5加2金卷系列答案
快乐5加2金卷系列答案(1)8g液态的CH3OH在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出Q kJ的热量。试写出液态CH3OH燃烧热的热化学方程式 。
(2)在化学反应过程中,破坏旧化学键需要吸收能量,形成新化学键又会释放能量。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | 391 | 945 |
已知反应N2+3H2=2NH3 ΔH=a KJ/mol。
试根据表中所列键能数据计算a的数值为: 。
(3)已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5 kJ/mol
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599 kJ/mol
根据盖斯定律,由C(s,石墨)和H2(g)生成1 mol C2H2(g)反应的热化学方程式: 。
 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1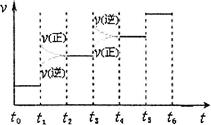
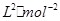 mol;
mol;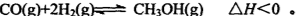

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
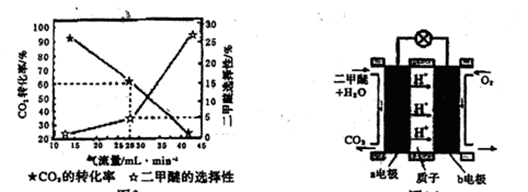
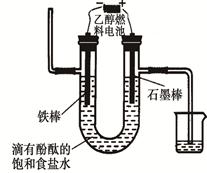
 2CO2(g)+ N2(g)。△H<0
2CO2(g)+ N2(g)。△H<0
 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol  2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。
2NH3(g),反应过程的能量变化如图所示。已知N2(g)与H2(g)反应生成17 g NH3(g),放出46.1 kJ的热量。