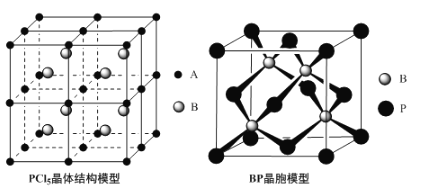
题目内容
【题目】A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):
A![]() B
B![]() C
C
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为___________(填元素符号)
(2)若D是金属,C溶液在储存时应加入少量金属D,其理由是(用必要的文字和离子方程式表示)______
(3)若A、B、C为含同一种金属元素的无机化合物,且三种物质中有一种是白色不溶物。在溶液中A和C反应生成B。请写出B转化为C的所有可能的离子力程式_________、_________
(4)某一离子反应体系有反应物和产物共以下六种:MnO4-、H+、O2、H2O、H2O2、Mn2+。
①写出该氧化还原反应的离子方程式_______
②溶液随着酸性的增强氧化性不断增强,应选择_________(选填“稀硫酸”或“浓盐酸”)进行KMnO4溶液的酸化。
③如反应转移了0.6mo1电子,则产生的气体在标准状况下体积为__________
(5)一份溶液中可能含有K+、Al3+、Mg2+、Fe2+、 H+、NH4+、Cl-、HCO3-、ClO-、AlO2-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
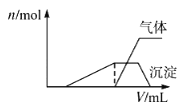
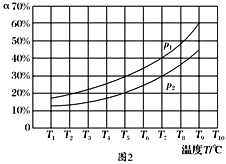
往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;则该溶液中一定存在的离子是_______,一定不存在的离子是________。
【答案】Na 2Fe3++ Fe=3Fe2+ Al(OH)3+3H+=Al3++3H2O Al(OH)3+ OH-=AlO2-+2H2O 2MnO4-+6H++5H2O2=2Mn2++5O2↑+8 H2O 稀硫酸 6.72 L Al3+、H+、NH4+、Cl- Mg2+、Fe2+、HCO3-、ClO-、AlO2-
【解析】
(1)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知A为Na,B为Na2O,D为O2,C为Na2O2;
(2)若D为金属,由转化关系可知为变价金属,应为Fe,则C含有Fe2+,具有还原性;
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成B.判断为:Al3+→Al(OH)3→![]() ,D为OH-;或
,D为OH-;或![]() →Al(OH)3→Al3+,D为H+;
→Al(OH)3→Al3+,D为H+;
(4)由H2O2→O2知,双氧水在反应中作还原剂,所以还必须有氧化剂参加反应,在反应中得电子化合价降低,根据化合价知,高锰酸根离子作氧化剂,还原产物是锰离子,同时反应后生成水,反应的离子方程式为:![]() ,结合离子方程式解答;
,结合离子方程式解答;
(5)根据产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(V)的关系的图示可以知道,刚加入氢氧化钠溶液时,没有产生沉淀;之后产生了沉淀,且沉淀完全溶解;沉淀溶解前产生了气体,该气体一定是氨气,以上分析依据,分别对离子存在情况作出判断。
(1)D是具有氧化性的单质,A元素属于短周期主族金属元素,根据反应关系可知A为Na,B为Na2O,D为O2,C为Na2O2;
(2)若D为金属,由转化关系可知为变价金属,应为Fe,则C含有Fe2+,具有还原性,保存时应加入少量Fe,防止被Fe2+空气氧化,原理是2Fe3++Fe=3Fe2+;
(3)若A、B、C为含同一种金属元素的无机化合物,在溶液中A和C反应生成B,判断为:Al3+→Al(OH)3→![]() ,A为Al3+,B为Al(OH)3,C为
,A为Al3+,B为Al(OH)3,C为![]() ,D为NaOH;或
,D为NaOH;或![]() →Al(OH)3→Al3+,A为
→Al(OH)3→Al3+,A为![]() ,B为Al(OH)3,C为Al3+,D为H+;B转化为C的离子方程式为:
,B为Al(OH)3,C为Al3+,D为H+;B转化为C的离子方程式为:![]() ;Al(OH)3+3H+=Al3++3H2O;
;Al(OH)3+3H+=Al3++3H2O;
(4)①由上述分析可知,该氧化还原反应离子方程式为:![]() ;
;
②高锰酸钾具有强氧化性,可氧化盐酸生成氯气,应用稀硫酸酸化;
③![]() 反应中,Mn元素化合价由+7价降低到+2价,由方程式可知生成5mol氧气转移10mol电子,则如反应转移了0.6mo1/span>电子,产生的氧气0.3mol,气体在标准状况下体积为0.3mol×22.4L/mol=6.72L;
反应中,Mn元素化合价由+7价降低到+2价,由方程式可知生成5mol氧气转移10mol电子,则如反应转移了0.6mo1/span>电子,产生的氧气0.3mol,气体在标准状况下体积为0.3mol×22.4L/mol=6.72L;
(5)根据图示,开始时没有沉淀生成,说明溶液中H+,一定没有ClO、![]() 、
、![]() ;随后出现沉淀,且沉淀完全溶解了,说明沉淀是氢氧化铝,溶液中一定含有Al3+,因Al3+与
;随后出现沉淀,且沉淀完全溶解了,说明沉淀是氢氧化铝,溶液中一定含有Al3+,因Al3+与![]() 、ClO-能够发生反应,则一定没有
、ClO-能够发生反应,则一定没有![]() 、ClO-;氢氧化铝溶解前生成了气体,该气体一定是氨气,故溶液中一定含有
、ClO-;氢氧化铝溶解前生成了气体,该气体一定是氨气,故溶液中一定含有![]() ;最终沉淀完全溶解,因此溶液中一定不含Mg2+、Fe2+;故答案为:Al3+、H+、
;最终沉淀完全溶解,因此溶液中一定不含Mg2+、Fe2+;故答案为:Al3+、H+、![]() 、Cl-;Mg2+、Fe2+、
、Cl-;Mg2+、Fe2+、![]() 、ClO-、
、ClO-、![]() 。
。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】下列实验现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向盛有高锰酸钾酸性溶液的试管中通入足量的乙烯后静置 | 溶液的紫色逐渐褪去,静置后溶液分层 |
B | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中产生浓烟并有黑色颗粒产生 |
C | 向盛有饱和硫代硫酸钠溶液的试管中滴加稀盐酸 | 有刺激性气味气体产生,溶液变浑浊 |
D | 向盛有FeCl3溶液的试管中加过量铁粉,充分振荡后加1滴KSCN溶液 | 黄色逐渐消失,加KSCN后溶液颜色不变 |
A. AB. BC. CD. D