题目内容
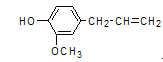
【题目】下列分子中所有碳原子不可能在同一平面上的是( )
A. 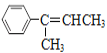 B.
B. ![]() C.
C. 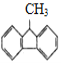 D.
D. 
【答案】C
【解析】
常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行分析。
A、分子中含有一个苯环,每个苯环上的碳原子一定共面,分子中含有一个碳碳双键,与碳碳双键相连的三个碳原子一定共面,苯环和碳碳双键通过可以旋转的碳碳单键相连,所有碳原子可能共面,故A不选;
B、![]() 可以看成是中间的苯环与两个苯环各共用两个碳原子形成的,分子中所有的碳原子都处在同一平面上,故B不选;
可以看成是中间的苯环与两个苯环各共用两个碳原子形成的,分子中所有的碳原子都处在同一平面上,故B不选;
C、分子中含有两个苯环,每个苯环上的碳原子一定共面,但是甲基相连的碳原子是烷烃的结构,是四面体构型,一定不会共面,该分子中的所有碳原子不可能都处在同一平面上,故C选;
D、 分子中含有两个苯环,每个苯环上的碳原子一定共面,两个乙基上的碳碳单键可以通过旋转使碳与苯环处于同一平面,所以该分子中的所有碳原子可能都处在同一平面上,故D不选;
分子中含有两个苯环,每个苯环上的碳原子一定共面,两个乙基上的碳碳单键可以通过旋转使碳与苯环处于同一平面,所以该分子中的所有碳原子可能都处在同一平面上,故D不选;
故选C。

 名校课堂系列答案
名校课堂系列答案【题目】下表是几种弱酸常温下的电离平衡常数:
CH3COOH | H2CO3 | H2S | H3PO4 |
1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=9.1×10-8 K2=1.1×10-12 | K1=7.5×10-3 K2=6.2×10-8 K3=2.2×10-13 |
则下列说法中不正确的是( )
A. 碳酸的酸性强于氢硫酸
B. 多元弱酸的酸性主要由第一步电离决定
C. 常温下,加水稀释醋酸,![]() 增大
增大
D. 向弱酸溶液中加少量NaOH溶液,电离常数不变
【题目】下表所列的是五种短周期元素的原子半径及主要化合价(已知铍的原子半径为0.089nm)。
元素代号 | A | B | C | D | E |
原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
(1)比较A、B、E三种元素的简单离子的离子半径大小___(用对应元素离子符号表示)。
(2)A元素简单离子的结构示意图为__,B元素位于周期表中第__周期__族。
(3)B的最高价氧化物对应水化物与C的最高价氧化物对应水化物反应的离子方程式为__。
(4)上述五种元素的最高价氧化物对应水化物中酸性最强的是__(填化学式)。
(5)C、E形成的化合物为__(填化学式)。
(6)用电子式表示A和D形成化合物的过程___。