题目内容
A、B、C、D四种元素处于同一周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。
(1)C原子的价电子排布式为 。
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号) 。
(3)B的单质分子中存在 个 键。
键。
(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于 晶体,其硬度比金刚石 (填“大”或“小”)。
(5)A的气态氢化物的沸点在同族中最高的原因是 。
(1)C原子的价电子排布式为 。
(2)A、B、C三种元素原子的第一电离能由大到小的顺序是(写元素符号) 。
(3)B的单质分子中存在 个
 键。
键。(4)D和B形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于 晶体,其硬度比金刚石 (填“大”或“小”)。
(5)A的气态氢化物的沸点在同族中最高的原因是 。
(1)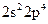 。(2分)(2)F>N>O(1分)(3)2(1分)(4)原子(1分)大(1分) (5)HF分子之间可以形成氢键从而使熔沸点升高(2分)
。(2分)(2)F>N>O(1分)(3)2(1分)(4)原子(1分)大(1分) (5)HF分子之间可以形成氢键从而使熔沸点升高(2分)
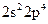 。(2分)(2)F>N>O(1分)(3)2(1分)(4)原子(1分)大(1分) (5)HF分子之间可以形成氢键从而使熔沸点升高(2分)
。(2分)(2)F>N>O(1分)(3)2(1分)(4)原子(1分)大(1分) (5)HF分子之间可以形成氢键从而使熔沸点升高(2分)略

练习册系列答案
相关题目